1 引言
这里,
这里,
在模型(1.2) 中, 文献[7] 假设细胞免疫过程遵循质量作用原理, 即每个T细胞对被感染靶细胞的清除率是恒定的. 然而, 文献[9] 中的报道表明微寄生虫感染率是随寄生虫剂量增加的增长函数(即, 形状呈S型), 文献[9–11] 中的研究也说明比起简单的双线性函数, 一些非线性函数可以在细胞免疫过程中更好地再现饱和效应. 基于此, 文献[4] 修改了具有CTL免疫反应的病毒感染模型, 用非线性函数
其中,
系统(1.3) 的初始条件如下
其中
2 解的正性和最终有界性
本节我们将讨论系统(1.3) 解的适定性问题. 根据泛函微分方程基本理论[14]可知系统(1.3) 存在满足初始条件(1.4) 的唯一解. 下面将证明系统(1.3) 解的正性和最终有界性.
定理2.1 对于
证 先证明解的非负性. 假设
故对于任意
下面证明解的最终有界性. 定义
沿系统(1.3) 计算
其中,
从而, 对任意
令
则有
综上所述, 系统(1.3) 满足初始条件(1.4) 的解非负且最终有界.证毕.
通过上述分析我们知道, 集合
是系统(1.3) 的正不变集.
3 可行平衡点和病毒感染基本再生率
本节我们计算系统(1.3) 的病毒感染基本再生率并研究各可行平衡点的存在性.
计算
易得
故由
这里,
这里,
4 可行平衡点的稳定性
4.1 可行平衡点的局部渐近稳定性
在本小节, 我们将通过分析对应特征方程根的分布来研究系统(1.3) 各可行平衡点的局部渐近稳定性.
定理4.1 当
证 系统(1.3) 在
显然,
当
故当
当
分离上述方程的实部和虚部并整理得
将(4.3) 的两个方程两边同时平方再相加得
令
故当
定理4.2 当
证 系统(1.3) 在平衡点
设
由
将(4.6) 和(4.7) 式代入(4.5)式并计算可得
又由(3.1)式有
将上述等式代入(4.8) 式并整理得
比较方程(4.5) 和不等式(4.9) 可知:
4.2 可行平衡点的全局渐近稳定性
在本小节, 我们将通过构造适当的Lyapunov泛函和应用LaSalle不变性原理研究系统(1.3) 各可行平衡点的全局渐近稳定性.
定理4.3 当
证 构造如下Lyapunov泛函
其中
由此可得,
定理4.4 当
证 构造如下Lyapunov泛函
沿系统(1.3) 的解计算
由此可得,
5 敏感性分析
本节将对系统(1.3) 的病毒感染基本再生率
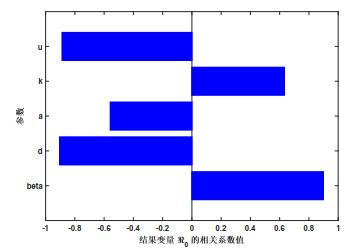
根据文献[17], 我们将采用LHS (Latin hypercube sampling) 和PRCCs (Partial rank correlation coefficients) 对病毒感染基本再生率
图 1
从图 1中可以看出:
6 结论
本文研究了一类具有饱和发生率、CTL免疫反应、免疫损害和胞内时滞的HIV感染动力学模型. 首先, 证明了系统解的非负性和最终有界性; 之后, 通过下一代矩阵法得到了系统的病毒感染基本再生率; 通过分析相应特征方程根的分布讨论了系统各可行平衡点的局部渐近稳定性; 通过构造适当的Lyapunov泛函和应用LaSalle不变性原理证明了系统(1.3) 的全局动力学性态由病毒感染基本再生率完全确定: 当病毒感染基本再生率小于1时, 病毒未感染平衡点全局渐近稳定; 当病毒感染基本再生率大于1时, 病毒感染平衡点全局渐近稳定.
参考文献
Virus dynamics and drug therapy
DOI:10.1073/pnas.94.13.6971 [本文引用: 2]
HIV-1 evolution and disease progression
DOI:10.1126/science.274.5289.1008 [本文引用: 1]
Global stability of an HIV-1 infection model with saturation infection and intracellular delay
DOI:10.1016/j.jmaa.2010.08.055 [本文引用: 2]
Complete dynamical analysis for a nonlinear HTLV-I infection model with distributed delay, CTL response and immune impairment
Dynamics analysis of a delayed viral infection model with immune impairment
DOI:10.1016/j.apm.2011.03.043 [本文引用: 3]
Threshold dynamics of an HIV-1 model with both viral and cellular, cell-mediated and humoral immune responses
DOI:10.3934/mbe.2019015 [本文引用: 3]
Stability and Hopf bifurcation of a HIV infection model with CTL-response delay
DOI:10.1016/j.camwa.2011.08.022 [本文引用: 4]
Defining CTL-induced pathology: implications for HIV
DOI:10.1006/viro.2000.0399 [本文引用: 1]
Dose effects and density-dependent regulation of two microparasites of Daphnia magna
Which of our modeling predictions are robust?
Persistent virus infection despite chronic cytotoxic T-lymphocyte activation in gamma interferon-deficient mice infected with lymphocytic choriomeningitis virus
DOI:10.1128/JVI.74.22.10304-10311.2000 [本文引用: 1]
Virus dynamics: the effect of target cell limitation and immune responses on virus evolution
Dynamics analysis of a delayed viral infection model with logistic growth and immune impairment
Reproduction numbers and sub-threshold endemic equilibria for compartmental models of disease transmission
DOI:10.1016/S0025-5564(02)00108-6 [本文引用: 2]
A methodology for performing global uncertainty and sensitivity analysis in systems biology