引言
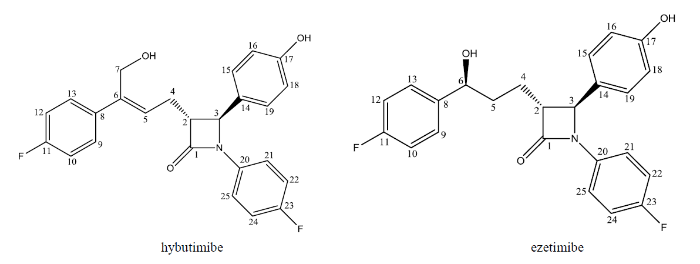
海博麦布是由浙江海正药业股份有限公司自主研发的1类新药,于2021年批准上市,是国内近二十年唯一获批上市的心血管1类新药,全球第二款胆固醇吸收抑制剂,用于治疗原发性高胆固醇血症疾病,化学名为1-(4-氟苯基)-3(R)-[3-(4-氟苯基)-4-羟基丁基-2(Z)-烯]-4(S)-(4-羟基苯基)-2-氮杂环丁烷酮,分子结构如图1所示[1].目前,国内外关于海博麦布的研究主要是工艺制备、晶型和药理学[1⇓⇓-4],完整的波谱学数据和结构解析还未见报道.本文采用紫外吸收光谱(UV光谱)、红外光谱(IR光谱)、质谱(MS)和核磁共振波谱(NMR)等方法对海博麦布的结构进行解析,对其所有的1H和13C NMR信号进行详细的归属,从而提供完整的波谱数据,并通过差示扫描量热法(DSC)、热重分析(TGA)及粉末X-射线衍射(PXRD)分析对海博麦布的晶型进行研究[5⇓-7].依折麦布是全球第一个上市的胆固醇吸收抑制剂,与海博麦布结构类似,因此本文将两者的NMR数据进行了对比,二者结构见图1.
图1
1 实验部分
1.1 试剂
氘代氯仿(CDCl3, 99.8 atom%D)和氘代二甲亚砜(DMSO-d6,99.8 atom%D)购自北京伊诺凯公司;甲醇(色谱纯)购自MERCK公司.
1.2 样品制备[2]
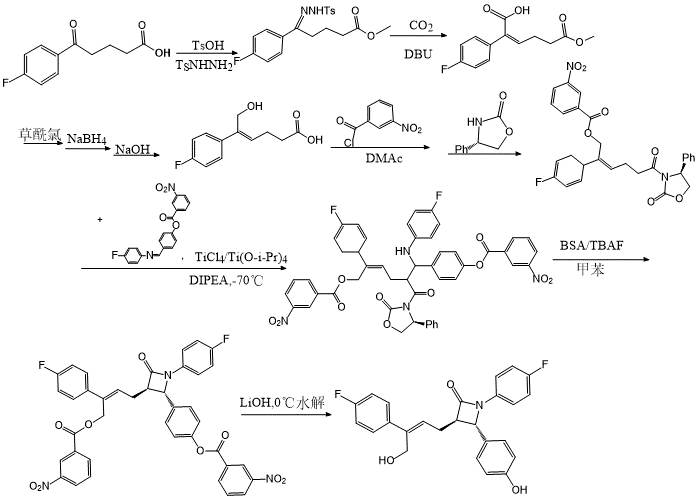
以羧酸酮酯为原料,经过格氏加成,立体选择性脱水,酯基还原,羟基保护,与手性助剂缩合后再与亚胺加成,最后关环,脱保护即得,合成路径见图2.以正庚烷和乙酸乙酯为溶剂重结晶,得到纯品.对纯化后的样品进行高效液相色谱(HPLC)分析,结果表明纯度为99.95%,符合结构鉴定所需纯度.将样品用丙酮溶解,放置于石油醚中扩散培养得到单晶.
图2
图2
海博麦布的合成路径.TsOH:对甲苯磺酸;TsNHNH2:对甲苯磺酰肼;DBU:1,8-二偶氮杂双螺环[5.4.0]十一-7-烯;DMAc: N, N-二甲基乙酰胺;DIPEA:N,N-二异丙基乙胺;BSA:N, O-双(三甲基硅基)乙酰胺;TBAF:四丁基氟化铵
Fig. 2
Synthetic route of hybutimibe. TsOH: p-toluenesulfonic acid; TsNHNH2: p-toluenesulfonyl hydrazide; DBU: 1,8-diazabicyclo [5.4.0]undec-7-ene; DMAc: N, N-dimethylacetamide; DIPEA: N,N-diisopropylethylamine; BSA: N,O-bis(trimethylsilyl)acetamide; TBAF: Tetrabutylammonium fluoride
1.3 测定条件
UV光谱采用SHIMADZU UV-2401PC紫外分光光度计获得,扫描波长范围为190~400 nm,仪器狭缝宽度为1 nm. IR光谱采用Bruker VECTOR22红外分光光度计测定,KBr压片,波数扫描范围为4 000~400 cm-1. MS采用Agilent 1260-6540QTOF液质联用仪,ESI源. TGA采用Perkin-Elmer TGA-4000热重分析仪测定,温度范围为30~300 ℃,升温速率为10 ℃/min. DSC采用NETSCH 200F3差热分析仪测定,温度范围为30~300 ℃,升温速率为10 ℃/min. PXRD分析采用Rigaku D/max2200 X射线衍射仪,电压为40 kV,电流为40 mA,Cu靶,范围为3˚~60˚,扫描速率为6˚/min. 单晶测试采用布鲁克Smart-apex-2单晶衍射仪,石墨单色仪,波长为1.541 78 Å.
1H NMR、13C NMR、1H-1H COSY、1H-13C HSQC和1H-13C HMBC均在Bruker Avance 400 MHz核磁共振波谱仪上完成.以CDCl3为溶剂,1H NMR、13C NMR的观测频率分别为400.133 MHz和100.623 MHz,一维谱谱宽分别为8 278 Hz和26 178 Hz. 二维谱均采用标准脉冲程序采集,1H-1H COSY的F2(1H)和F1(1H)维谱宽均为6 410 Hz,采集数据点阵t2*t1 = 2 048*128,累加次数10;1H-13C HSQC的F2(1H)和F1(13C)维谱宽分别为6 410 Hz和26 162 Hz,采集数据点阵t2*t1=2 048*256,累加次数10;1H-13C HMBC的F2(1H)和F1(13C)维谱宽分别为6 410 Hz和26 162 Hz,采集数据点阵t2*t1 = 4 096*128,累加次数40.
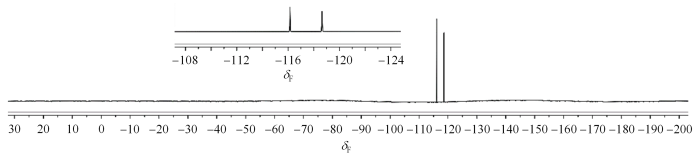
为了验证活泼质子的存在、氟原子个数及位置和相对空间构型,另以DMSO-d6为溶剂在Agilent 400M DD2核磁共振波谱仪上进行1H NMR、19F NMR和1H-1H NOESY实验,1H NMR的观测频率为399.77 MHz,谱宽为6 410 Hz;19F NMR的观测频率为376.13 MHz,谱宽为89 285.7 Hz;1H-1H NOESY的F2(1H)和F1(1H)维谱宽均为4 112Hz,采集数据点阵t2*t1 = 617*200,累加次数16.
2 结果与讨论
2.1 UV光谱分析
在甲醇溶液中,海博麦布样品的最大吸收波长为236.45 nm和202.95 nm,分别为苯环B和E吸收谱带.
2.2 IR光谱分析
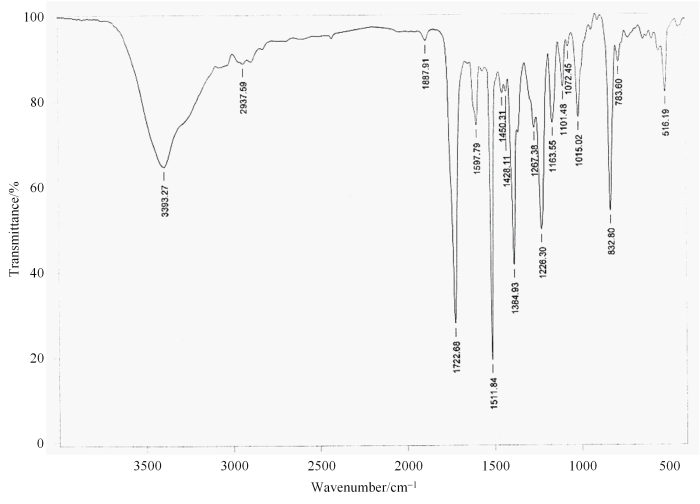
海博麦布的IR(cm-1):3 393(br, s),2 938(w),1 723(s),1 598(m),1 512(s),1 385(s), 1 226(s),1 164(m),1 015(m),833(m).3 393 cm-1强宽峰,为羟基O-H伸缩振动;2938 cm-1为亚甲基C-H伸缩振动;1 723 cm-1为酰胺基C=O伸缩振动;1 598~1 512 cm-1为苯环骨架伸缩振动;1 385 cm-1为羟基O-H弯曲振动;1 226 cm-1为C-F伸缩振动;1 164~1 015 cm-1为C-O伸缩振动;833 cm-1为不饱和C-H弯曲振动.
图3
2.3 MS谱图分析
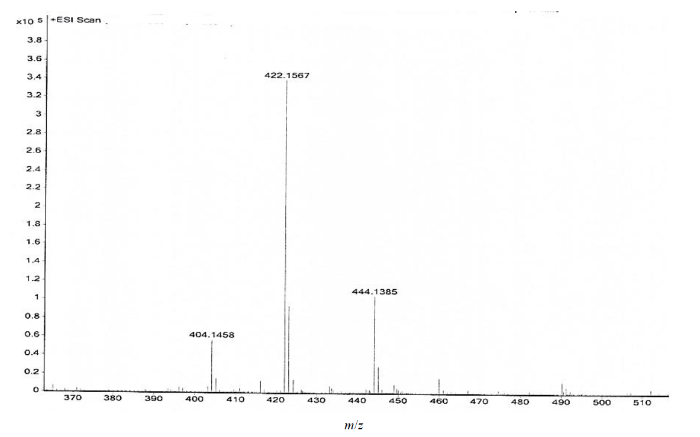
在正离子模式下得到m/z = 404.145 8的离子峰为[M-H2O+H]+的峰,m/z = 422.156 7的离子峰为[M+H]+的峰,m/z = 444.138 5的离子峰为[M+Na]+的峰,与海博麦布的元素组成C25H21F2NO3(与理论值偏差-1.09×10-6)相符.
图4
2.4 单晶结果
单晶检测结果表明本品为Z式,C-2为R构型,C-3为S构型.晶胞结构见图5.
图5
2.5 晶型分析
由TGA和DSC结果(见附件材料图S1和S2)可知,本品不含结晶水,熔点为154.3 ℃(onset).由PXRD结果(见附件材料图S3)可知,本品为结晶性粉末.
2.6 核磁共振谱图分析
2.6.1 信号归属
图6
图7
图8
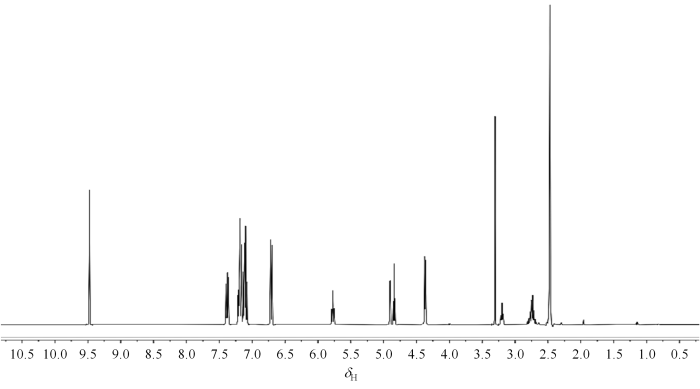
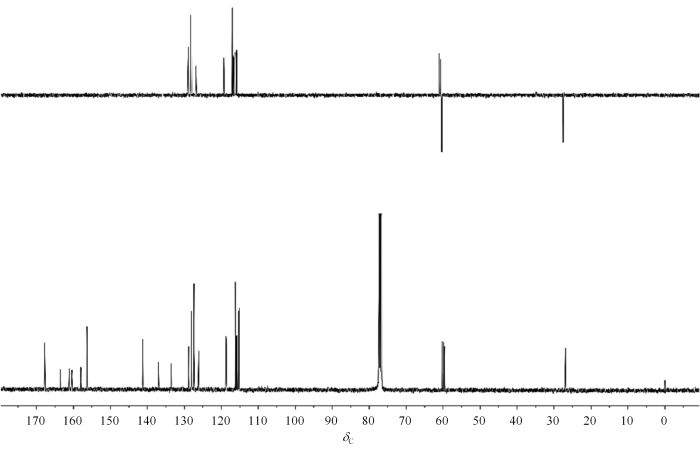
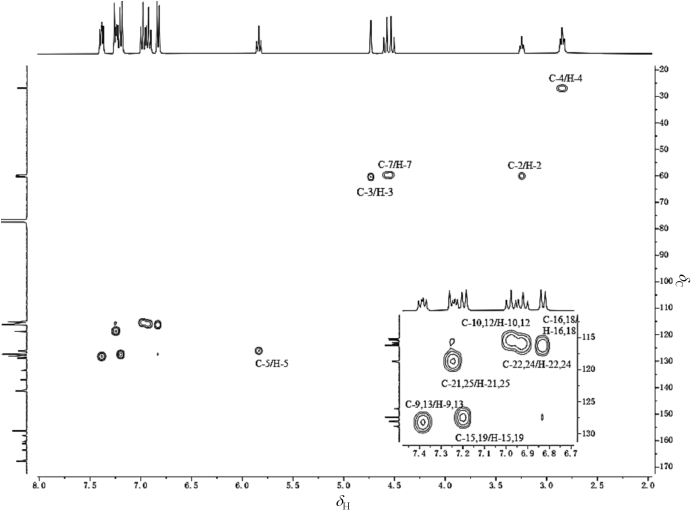
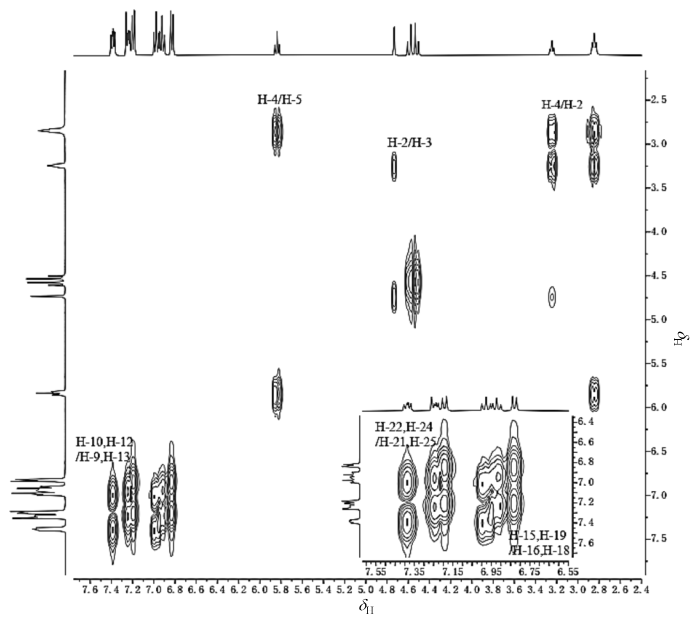
根据化学位移值的估算方法,结合DEPT谱(图9)和1H-13C HSQC谱(图10)可推知δC 59.6为C-7,δH 4.50、4.58为H-7.1H-1H COSY谱(图11)表明δH 2.85(2H,m)、3.25(1H,m)、4.73(1H,d,J=2.0 Hz)和5.84(1H,t,J=8.1 Hz)为一个自旋体系,有如下关系:δH 4.73↔3.25↔2.85↔5.84,其中δH 5.84在1H-13C HMBC谱(图12)上与C-7远程相关,可判断为H-5,δH 2.85、3.25、4.73则分别归属为H-4、H-2、H-3. 再根据1H-13C HSQC谱,δH 2.85、3.25、4.73分别与δC 26.9、59.9、60.3直接相连,可确定δC 26.9、59.9、60.3分别为C-4、C-2、C-3.1H-1H COSY谱表明,δH 6.84(2H,d,J=8.4 Hz)和δH 7.18(2H,d,J=8.4 Hz)相关,δH 6.92(2H,t,J=8.6 Hz)和δH 7.26(2H,dd,J=4.6/8.9 Hz)相关,δH 6.98(2H,t,J=8.6 Hz)和δH 7.38(2H,dd,J=5.5/8.5 Hz)相关,对应3个对位取代苯环上的3组氢,因为有2个苯环上对位取代为氟原子,受氟原子的耦合产生不同的峰形,所以结合峰形,可以推知δH 6.84和δH 7.18为对羟基苯的氢.根据1H-13C HSQC谱可知,δH 6.84与δC 116.2相连,δH 7.18与δC 127.4相连,再根据1H-13C HMBC谱,δC 116.2与δH 6.84远程相关,δC 127.4与δH 7.18和δH 4.73远程相关,可以推知δH 6.84为H-16、H-18,δC 116.2为C-16、C-18,δH 7.18为H-15、H-19,δC 127.4为C-15、C-19.对氟苯基上2组氢的归属则需要对其季碳归属后再确定.根据耦合常数和1H-13C HMBC谱,δC 137.0(d,J=4 Hz)与H-7和H-5远程相关,可以推知其为C-8,那δC 133.6(d,J=2 Hz)则可确定为C-20.由1H-13C HMBC谱可知,C-8还与δH 6.98相关,结合δH 6.98(2H,t,J=8.6 Hz)的峰形和耦合常数,可以推知其为H-10、H-12,δH 7.38(2H,dd,J=5.5/8.5 Hz)则为H-9、H-13,同理可以推知δH 6.92(2H,t,J=8.6 Hz)和δH 7.26(2H,dd,J=4.6/8.9 Hz)分别为H-22、H-24和H-21、H-25.根据氟对相邻苯环上碳原子耦合常数约为250 Hz,可以确定δC 159.2(d,J=243 Hz)、162.3(d,J=245 Hz)为与氟直接相连碳原子,再根据HMBC谱,δC 159.2与H-22、H-24、H-21、H-25远程相关,δC 162.3与H-10、H-12、H-9、H-13远程相关,可以确定为δC 159.2为C-23,δC 162.3为C-11.根据化学位移和HMBC谱,δC 167.8与H-2、H-3、H-4相关,可以确定为C-1;δC 156.3与H-15、H-19、H-16、H-18相关,可以确定为C-17;δC 141.2与H-4、H-5、H-7相关,可以确定为C-6;δC 128.8与H-2、H-16、H-18相关,可以确定为C-14.
图9
图9
海博麦布DEPT-135(上)和13C NMR(下)谱
Fig. 9
DEPT-135 (top) and 13C NMR (bottom) spectrum of hybutimibe
图10
图11
图12
图12
海博麦布的1H-13C HMBC谱(a)及其局部放大谱(b)
Fig. 12
1H-13C HMBC spectrum(a) and partial enlarged spectrum(b) of hybutimibe
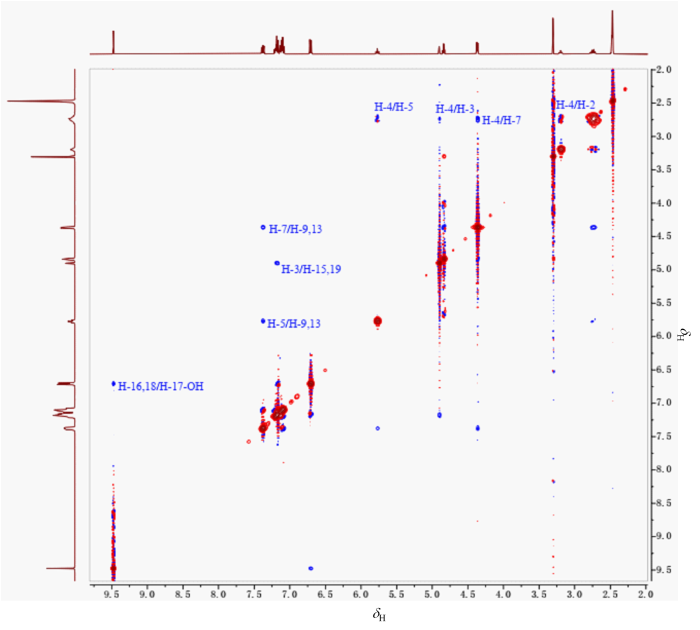
1H-1H NOESY(图13)中,H-4与H-7相关,H-5与H-9、H-13相关,推断双键为Z式.H-3的耦合常数为2.4 Hz,非对映异构体中H-3的耦合常数为5.5 Hz,与H-2和H-3二面角大小(海博麦布为136.7˚,非对映异构体为5.9˚)相符.
图13
综上,可以对海博麦布进行NMR信号归属,具体见表1.
表1 海博麦布样品的NMR信号归属*
Table 1
| Assignment | δC | DEPT | HMBC | δH | δH(DMSO-d6) | COSY | NOESY(DMSO-d6) |
|---|---|---|---|---|---|---|---|
| 4 | 26.9 | CH2 | 3.25(H2),4.73(H3), 5.84(H5) | 2.85(m,2H) | 2.75(m,2H) | 3.25(H2), 5.84(H5) | 3.20(H2), 4.36(H7), 4.90(H3), 5.77(H5) |
| 7 | 59.6 | CH2 | 5.84(H5) | 4.50,4.58 (d,J=12.4 Hz,2H) | 4.36 (d,J=5.3 Hz,2H) 4.84 (OH,t,J=5.3 Hz,1H) | / | 2.75(H4), 7.38(H9,H13) |
| 2 | 59.9 | CH | 4.73(H3),5.84(H5) | 3.25(m,1H) | 3.20(m,1H) | 2.85(H4), 4.73(H3) | 2.75(H4) |
| 3 | 60.3 | CH | 2.85(H4),3.25(H2), 7.18(H15,H19) | 4.73(d,J=2.0 Hz,1H) | 4.90 (d,J=2.4 Hz,1H) | 3.25(H2) | 2.75(H4), 7.19(H15,H19) |
| 10,12 | 115.3(d,J=22 Hz) | CH | 6.98(H10,H12), 7.38(H9,H13) | 6.98(t,J=8.7 Hz,2H) | 7.12 (m,2H) | 7.38(H9,H13) | / |
| 22,24 | 115.9(d,J=23 Hz) | CH | 6.92(H22,H24) | 6.92(t,J=8.6 Hz,2H) | 7.12(m,2H) | 7.26(H21,H25) | / |
| 16,18 | 116.2 | CH | 6.84(H16,H18) | 6.84(d,J=8.4 Hz,2H) | 6.70 (d,J=8.6 Hz,1H) | 7.18(H15,H19) | / |
| 21,25 | 118.7(d,J=8Hz) | CH | 7.26(H21,H25) | 7.26(dd,J=4.6/8.9 Hz,2H) | 7.19(m,2H) | 6.92(H22,H24) | / |
| 5 | 126.1 | CH | 2.85(H4),3.25(H2), 4.50(H7),4.58(H7) | 5.84(t,J=8.1 Hz,1H) | 5.77 (t,J=7.7 Hz,1H) | 2.85(H4) | 7.38(H9,H13) |
| 15,19 | 127.4 | CH | 4.73(H3), 7.18(H15,H19) | 7.18(d,J=8.4 Hz,2H) | 7.19(m,2H) | 6.84(H16,H18) | 4.90(H3) |
| 9,13 | 128.1(d,J=8Hz) | CH | 7.38(H9,H13) | 7.38(dd,J=5.5, 8.5 Hz,2H) | 7.38(m,2H) | 6.98(H10,H12) | 4.36(H7), 5.77(H5) |
| 14 | 128.8 | C | 3.25(H2), 6.84(H16,H18) | / | / | / | / |
| 20 | 133.6(d,J=2Hz) | C | 6.92(H22,H24), 7.26(H21,H25) | / | / | / | / |
| 8 | 137.0 ( d,J=4Hz) | C | 4.50(H7),4.58(H7), 5.84(H5), 6.98(H10,H12) | / | / | / | / |
| 6 | 141.2 | C | 2.85(H4),4.50(H7), 4.58(H7),5.84(H5), 7.38(H10,H12) | / | / | / | / |
| 17 | 156.3 | C | 6.84(H16,H18), 7.18(H15,H19) | / | 9.48(OH,s,1H) | / | 6.70(H16,H18) |
| 23 | 159.2 (d,J=243Hz) | C | 6.92(H22,H24), 7.26(H21,H25) | / | / | / | / |
| 11 | 162.3(d,J=245Hz) | C | 6.98(H10,H12), 7.38(H9,H13) | / | / | / | / |
| 1 | 167.8 | C | 2.85(H4),3.25(H2), 4.73(H3) | / | / | / | / |
*:除括号内特别标注,其余实验数据均以CDCl3为溶剂.
2.6.2 与依折麦布NMR数据对比
海博麦布和依折麦布(结构见图1)结构区别主要在海博麦布5、6号位变为双键,6号位的羟基变为羟甲基,体现在NMR图谱上是多了一个连羟基的仲碳(δC 59.6, δH 4.50, 4.58),5号位由一个饱和仲碳(δC 36.36, δH 1.73)变为不饱和叔碳(δC 126.1, δH 5.84),6号位由连羟基的饱和叔碳(δC 71.05, δH 4.50)变为不饱和季碳(δC 141.2),8号位季碳因为苯环与5、6号位双键形成共轭,化学位移向高场移动(δC 142.19 vs. 137.0),4号位氢受相邻双键影响向低场移动(δH 1.73, 1.83 vs. 2.85).具体数据见表2.
表2 海博麦布和依折麦布[8]NMR数据比较(溶剂均为CDCl3)
Table 2
| Assignment | δC | δH | |||
|---|---|---|---|---|---|
| hybutimibe | ezetimibe | hybutimibe | ezetimibe | ||
| 4 | 26.9(CH2) | 24.50(CH2) | 2.85(m, 2H) | 1.73, 1.83 | |
| 7 | 59.6(CH2) | / | 4.50, 4.58(d, J=12.4 Hz, 2H) | ||
| 2 | 59.9(CH) | 59.40(CH) | 3.25(m, 1H) | 3.09 | |
| 3 | 60.3(CH) | 59.58(CH) | 4.73(d, J =2.0 Hz, 1H) | 4.81 | |
| 10,12 | 115.3(CH, 22) | 114.64(CH, 21.0) | 6.98(t, J =8.7 Hz, 2H) | 7.11 | |
| 22,24 | 115.9(CH, 23) | 115.79(CH, 22.5) | 6.92(t, J=8.6 Hz, 2H) | 7.13 | |
| 16,18 | 116.2(CH) | 115.71(CH) | 6.84(d, J=8.4 Hz, 2H) | 6.76 | |
| 21,25 | 118.7(CH, 8) | 118.22(CH, 8.0) | 7.26(dd, J=4.6/8.9 Hz, 2H) | 7.22 | |
| 5 | 126.1(CH) | 36.36(CH2) | 5.84(t, J=8.1 Hz, 1H) | 1.73 | |
| 15,19 | 127.4(CH) | 127.52(CH) | 7.18(d, J=8.4 Hz, 2H) | 7.18 | |
| 9,13 | 128.1(CH, 8) | 127.50(CH, 9.0) | 7.38(dd, J=5.5/8.5 Hz, 2H) | 7.32 | |
| 14 | 128.8(C) | 127.88(C) | / | ||
| 20 | 133.6(C, 2) | 133.98(C, 2.3) | / | ||
| 8 | 137.0(C, 4) | 142.19(C, 2.9) | / | ||
| 6 | 141.2(C) | 71.05(CH) | / | 4.50 | |
| 17 | 156.3(C) | 157.42(C) | / | 1.73, 1.83 | |
| 23 | 159.2(C, 243) | 157.05, 158.96(C, 240.2) | / | ||
| 11 | 162.3(C, 245) | 160.06, 161.98(C, 241.5) | / | 3.09 | |
| 1 | 167.8(C) | 167.33(C) | / | 4.81 | |
3 结论
本文通过IR光谱、UV光谱、MS和NMR波谱等方法对海博麦布的结构进行了全面的分析,IR图谱表明样品分子结构中含有羟基、亚甲基、酰胺基、苯环、氟等基团;UV图谱表明样品分子结构中含有苯环;高分辨MS推测分子式与海博麦布分子式相符,NMR氢谱、碳谱及二维谱等均与结构相符.通过DSC、TGA和PXRD分析,确证了海博麦布不含结晶水,为结晶性粉末.
利益冲突
无
附件材料(可在《波谱学杂志》期刊官网 http://magres.wipm.ac.cn 获取)
图S1 海博麦布TGA图
图S2 海博麦布DSC图
图S3 海博麦布PXRD图
参考文献
Spectroscopic data derived structure of lafutidine
[J].
拉呋替丁的波谱学数据和结构确证
[J].
Spectroscopic studies of delafloxacin meglumine
[J].
德拉沙星葡甲胺波谱学数据解析
[J].
Physicochemical characterization of ezetimibe and its impurities
[J].DOI:10.1016/j.molstruc.2011.02.020 URL [本文引用: 2]
海泽麦布中间体及其制备方法: PCT, WO2022262768
[P]. 2022-06-15.