引言
费托合成反应可将合成气(CO和H2混合物)经催化转化为烃类燃料和含氧化学品.费托合成反应产生的烃类燃料在一定程度上能确保能源供给安全,并减少对传统石油资源的依赖.其化学反应方程式如下:生成烷烃nCO+(2n+1)H2→CnH2n+2+nH2O;生成烯烃nCO+2nH2→CnH2n+nH2O;生成醇类nCO+2nH2→CnH2n+1OH+(n-1)H2O;生成醛类(n+1)CO+(2n+1)H2→CnH2n+1CHO+nH2O.可见,通过该反应每获取一个单元的CH2(摩尔质量14)烃类燃料,将无法避免地排放一单元反应生成水(H2O,摩尔质量18),即便是在理论转化率状态下,费托反应生成水的排放量也明显大于烃类燃料的生产规模.例如,以中国科学院山西煤炭化学研究所开发的铁基催化剂为核心技术,神华宁煤集团建成的年产400万吨煤制油项目,其费托合成生成的油水质量比约为1:1.6[1],每年的费托反应生成水量理论可达640万吨.更为严峻的问题在于:费托反应生成水中通常含有一定浓度的可溶性含氧有机化合物.例如,从中科合成油中试生产线获取的费托反应生成水,含有大量的醇类、醛类、酸类和酯类物质,其中甲醇浓度为1.24 wt.%、乙醇2.76 wt.%、正丙醇1.43 wt.%、正丁醇1.54 wt.%、丙酮0.36 wt.%、丁酮0.13 wt.%、乙酸1.45 wt.%、丙酸0.3 wt.%、其它有机物0.79 wt.%.由于这些含氧小分子的存在,费托反应生成水通常呈酸性、具有腐蚀性,会对环境造成一定的威胁,所以需处理以达到环保要求[2].常用的水处理技术,如物化预处理法、生化处理[3]、深度处理[4]、厌氧处理[5]、电解处理[6-8]和催化剂处理[9-11]技术,以及水处理材料,如活性炭、壳聚糖材料[12, 13],但在处理费托反应生成水过程中均表现出一定的局限性.例如,生化法对废水中的苯酚类及芳香类物质有较好的去除效果,但对醇、醛、酸、酮和酯等含氧有机小分子的去除效果较差.催化剂技术处理效率高,但高运行成本限制了其发展和应用.壳聚糖、活性炭等通常处理规模小.所以,迫切需要廉价易得、规模化的处理技术和材料来处理低浓度的费托反应生成水,降低其对环境的污染.
有研究[14]表明褐煤孔隙发达,表面和本体具有丰富的毛细管、裂缝、敞开和封闭孔,这些孔道可物理吸附特定尺寸的污染物分子.此外,褐煤中含有醇羟基(C-OH)、酚羟基(Ar-OH)、羧基(-COOH)、羰基(-C=O)、醚键(C-O-C)和甲氧基(O-CH3)等含氧官能,这些官能团对其表面性质,如亲水性、表面电性和表面作用等,都具有较大的影响,使褐煤成为吸附污染物的潜在物质.我们团队的前期研究发现:褐煤脱矿物质后获得的干酪根在处理含铬废水上表现出优异的性能[15],同时还发现Cr(Ⅵ)与干酪根中还原性物质发生氧化还原反应,且还原后的Cr(Ⅲ)通过-O-Cr-O-的作用固定在干酪根中,从而防止铬离子流失造成潜在环境污染[16, 17].可见,褐煤由于其吸附性能及价格低廉有望用于大批量处理费托反应生成水.腐殖酸(HA)是褐煤中有机质的主要成分,通常认为HA是一种以多元醌和多元酚等芳香类基团簇构成的高聚物,分子中含有大量的苯环、稠苯环和杂环,团簇上连接羧基、羟基、羰基、酚羟基、醌基、甲氧基等官能团,且团簇之间通过-O-、-CH2-、-NH-、-S-等桥键连接,呈现出一定的三维立体结构[18, 19].因此,HA表现出许多独特的物理化学性质,如酸性、亲水性、离子交换性、络合性、界面活性、氧化-还原性等,这些性质通常与吸附作用直接相关.HA通常可作为褐煤的模型化合物用于考察吸附性能[20].有研究表明HA能够有效吸附处理水相中的有机污染物,如芘[21]、1-萘酚[22]和萘丙胺[23],因此HA可以作为吸附剂处理费托反应生成水.
用HA处理费托反应生成水时,因费托反应生成水中含氧有机小分子种类繁多,导致作用方式多且复杂.因此,我们需从费托反应生成水中选择代表性的含氧有机物作为模型化合物,深入研究HA与模型化合物的作用方式及作用机理.费托反应生成水中含氧有机化合物羧酸和醇类化合物含量高,易溶于水且能稳定存在,正丁醇和丙酸的特有长度的烷基链和官能团使得其与HA能够相互作用,充分体现出分子形状和结构在与HA络合时起到的作用.本研究利用一维1H NMR化学位移滴定、T1和T2测试这些NMR技术研究费托反应生成水中的正丁醇、丙酸与HA之间的相互作用,揭示醇类和酸类化合物在相互作用过程中的差异性,以及HA浓度和溶液pH值对其相互作用的影响,进一步解释正丙醇、丙酸与HA的作用机理.
1 实验部分
1.1 仪器与试剂
仪器:Bruker AV-Ⅲ 400 MHz液体NMR谱仪,配备带有梯度场的5 mm PABBO BB/19F-1H/D变温探头.
试剂:腐殖酸钠(黄腐酸≥90%)购自上海阿拉丁试剂公司.正丁醇(分析纯,99.5%)和丙酸(分析纯,99.5%)购自国药集团化学试剂有限公司.DCl(20 wt.%,99.5% D原子)、NaOD(30 wt.%,99.5% D原子)、D2O(99.9% D原子)购自青岛腾龙微波科技有限公司.所有样品均未进一步纯化.
1.2 样品准备与实验方法
1.2.1 样品准备
以重水为溶剂,配制HA溶液,浓度为0.5 mg/mL.
以重水为溶剂,配制正丁醇和丙酸混合溶液,正丁醇和丙酸浓度均为0.5 mg/mL.
分别往1 mL的上述正丁醇和丙酸重水混合溶液中加入不同量(0.5、1、2、3、4、5、10、15、20、25、30、35、40、45、50 mg)的HA,混合均匀后,在摇床上室温反应48 h后,取500 μL反应液转移至5 mm NMR样品管中待测.
不同pH的正丁醇(0.5 mg/mL)和丙酸(0.5 mg/mL)混合溶液用DCl和NaOD溶液调配.
1.2.2 NMR实验
1H NMR测试的工作频率为400.13 MHz.测试温度为25 ℃,谱宽为8 012.82 Hz,采用标准脉冲程序.5 mm NMR滴定样品管中的待测样品都含有一定量的D2O,以D2O的残留质子信号进行定标(δH 4.70)[29].
1H的T1值测定采用的脉冲序列为t1ir,测试温度为25 ℃,测定参数如下:谱宽为4 000.00 Hz;中心频率为2 470.97 Hz;采样数据点阵t2×t1=32 768×16;累加次数8;正丁醇和丙酸的弛豫延迟值范围为3~30 s.使用CPMG(Carr-Purcell-Meiboom-Gill)脉冲序列获取1H的T2值,弛豫延迟值是最大T1值的5倍.弛豫时间重复测量2次,标准差均小于0.1 s.所有谱图使用Topspin 3.1软件测量和分析.
1.2.3 分子相关时间以及与HA结合的正丁醇和丙酸百分比的计算
分子相关时间
其中,系数
Simpson等[32]提出T1可用来计算与HA结合的正丁醇和丙酸的百分比(ρ):
其中,T1obsd表示观测溶液中,正丁醇、丙酸的T1测量值(单位为s);T1free表示没有加入HA时,正丁醇和丙酸的T1测量值;T1complex为与HA完全络合时,正丁醇和丙酸的T1测量值.使用Origin 2021软件对(2)式计算的关系式进行线性拟合.
2 结果与讨论
2.1 HA的1H NMR谱图
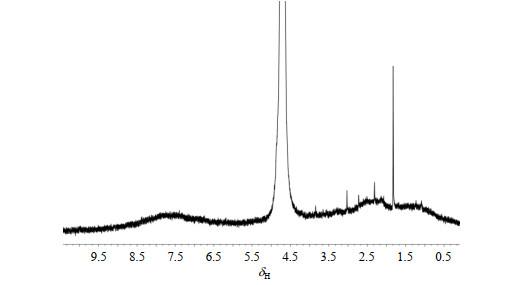
我们首先获取了HA溶液的1H NMR谱图(图 1).由谱图可知HA中质子所处化学环境复杂,1H NMR谱图重叠严重.δH 1.50~4.00之间的尖锐信号可能来自于HA制备过程中残留的溶剂小分子,δH 4.70是溶剂残留信号峰,δH 7.50附近的宽包信号为苯环上的质子,δH 2.40附近为与羧基、酮羰基、醛基相连的亚甲基,说明HA具有芳香环结构和含氧结构区.HA的含氧结构区和脂肪区促进其疏水区域的形成,能够将疏水特性的正丁醇和丙酸包裹在内,使得正丁醇和丙酸从自由状态逐渐向结合态转变,从而达到吸附的目的.
图1
图1
HA溶液的1H NMR谱(0.5 mg/mL,D2O,25 ℃)
Fig.1
1H NMR of HA solution with a concentration of 0.5 mg/mL (D2O, 25 ℃)
2.2 HA与正丁醇、丙酸的相互作用
2.2.1 1H NMR滴定实验
1H NMR信号的化学位移和峰宽对氢原子核周围的化学环境变化非常敏感[35].因此,我们首先利用化学位移滴定法检测了HA与正丁醇、丙酸的相互作用.图 2是正丁醇、丙酸与不同含量的HA混合溶液的1H NMR堆叠图.可以看出随着HA浓度增加,正丁醇与丙酸的质子信号逐渐变宽.HA浓度为0~5 mg/mL时,正丁醇的H-1、H-4和丙酸的H-5、H-6裂分清晰可辨.随着HA浓度逐渐增大至20 mg/mL时,H-1和H-4渐变为宽包信号;但H-5、H-6裂分仍然可辨,半峰宽没有明显变化.当HA浓度大于20 mg/mL,正丁醇的H-1、H-2、H-3、H-4的峰宽变化不再明显;而丙酸的H-5、H-6在HA浓度达到30 mg/mL后,峰宽变化才不再显著.而且,正丁醇的质子化学位移受HA浓度变化影响很小,几乎没有发生化学位移变化[36].但HA浓度在0~20 mg/mL范围内,丙酸的H-5和H-6化学位移向高场移动,其中H-6化学位移向高场移动的幅度较大(△δH=0.21 ppm),H-5化学位移变化较小(△δH=0.04 ppm);当HA浓度大于20 mg/mL后,H-5和H-6化学位移几乎不再变化.根据之前的报道[36],HA与疏水性有机化合物非共价相互作用时,小分子运动受限,一般都会导致谱峰变宽,而有机化合物的质子化学位移几乎保持不变,由以上分析可以初步推断HA与正丁醇之间为非共价相互作用,而丙酸化学位移的变化的原因需进一步探讨.
图2
图2
正丁醇、丙酸与不同含量的HA混合溶液的1H NMR堆叠图(正丁醇和丙酸浓度均为0.5 mg/mL,HA浓度为0~50 mg/mL)
Fig.2
1H NMR spectra of 0.5 mg/mL n-butanol and 0.5 mg/mL propionic acid mixture with different concentrations of HA (0~50 mg/mL)
图3
图3
正丁醇、丙酸与不同含量的HA混合溶液的pH(正丁醇和丙酸浓度均为0.5 mg/mL,HA浓度为0~30 mg/mL)
Fig.3
The pH values of 0.5 mg/mL n-butanol and 0.5 mg/mL propionic acid mixture with different concentrations of HA (0~30 mg/mL)
为了进一步验证猜想,我们通过DCl和NaOD调配无HA加入的正丁醇和丙酸的混合溶液,使其pH达到6.2,与加入浓度为20 mg/mL的HA的正丁醇和丙酸混合液的pH值相等,并测试了这一溶液的1H NMR谱图(图 4).与pH为3.6的正丁醇和丙酸溶液(δH-6 2.30,δH-5 0.99)相比,调配pH至6.2的正丁醇和丙酸混合溶液中,丙酸质子的化学位移向高场移动(δH-6 2.10,δH-5 0.96),并且与HA(20 mg/mL)、正丁醇和丙酸混合液中丙酸的质子化学位移相同(δH-6 2.10,δH-5 0.96).有研究[37]对比了溶液pH分别为5.2和7.0时,草甘膦与HA的相互作用,发现溶液pH为7.0时,草甘膦中靠近磷酸根的质子的化学位移较pH为5.0时向高场移动.另外,由于HA浓度的增大,丙酸的核被HA的疏水空腔所包围,磁屏蔽增强,导致其化学位移向高场移动.因此,丙酸H-5和H-6化学位移向高场移动,一部分归因于溶液的pH逐渐变大,另一部分是由于丙酸与HA的相互作用逐渐增大.而且由于H-6靠近羧基,其化学位移向高场移动较H-5大.
图4
图4
溶液pH对正丁醇和丙酸化学位移的影响.(a) 正丁醇和丙酸混合溶液,pH=3.6;(b) DCl和NaOD调配后的正丁醇和丙酸混合溶液,pH=6.2;(c) 添加浓度为20 mg/mL HA后的正丁醇和丙酸溶液,pH=6.2
Fig.4
The effect of solution pH on the chemical shift of n-butanol and propionic acid. (a) The original solution of n-butanol and propionic acid, pH=3.6; (b) Solution of n-butanol and propionic acid after pH adjustment with DCl and NaOD, pH=6.2; (c) Solution of n-butanol and propionic acid after addition of 20 mg/mL HA, pH=6.2
2.2.2 1H弛豫时间(T1和T2)的测定
图 5展现了正丁醇和丙酸的T1值与HA的浓度关系.同一溶液中,正丁醇所有质子(H-1~H-4)的T1值相近,因此可以推断与HA相互作用时,正丁醇的所有质子所处的化学环境相近;而丙酸的H-5和H-6的T1值不一致,表明丙酸与HA相互作用时,其质子所处的化学环境不一样.未加入HA时,正丁醇H-4和丙酸H-6的T1值分别为4.09 s和5.71 s;当HA浓度为1 mg/mL时,H-4和H-6的T1值分别迅速下降至1.25 s和1.53 s;当HA浓度5 mg/mL时,H-4和H-6的T1值分别继续下降至0.42 s和0.77 s.可见正丁醇H-4和丙酸H-6的T1值在HA浓度为0~5 mg/mL时,下降较快.但是当HA浓度为5~15 mg/mL时,正丁醇H-4的T1值从0.42 s下降到0.09 s、丙酸H-6的T1值从0.77 s降到0.63 s,下降速率均趋缓,但丙酸T1要比相同HA浓度下正丁醇的T1大.HA浓度升高为20 mg/mL时,正丁醇H-4与丙酸H-6的T1值几乎不再降低,趋于平衡.对于正丁醇的其它质子,随HA浓度增加,其T1的下降趋势与H-4一致.正丁醇和丙酸所有质子的T1平均下降幅度分别为98.5%和90.2%.T1值的显著下降和正丁醇、丙酸与HA的相互作用强度一致,正丁醇的T1值下降幅度较丙酸大,即正丁醇与HA的相互作用较丙酸与HA作用强.
图5
图5
丁醇、丙酸与不同含量的HA混合溶液中各质子的T1值(正丁醇和丙酸浓度均为0.5 mg/mL,HA浓度为0~30 mg/mL)
Fig.5
T1 values of protons in 0.5 mg/mL n-butanol and 0.5 mg/mL propionic acid mixture with different concentrations of HA (0~30 mg/mL)
表1 正丁醇和丙酸质子的T1和T2值随HA浓度的变化
Table 1
| CHA/(mg/mL) | T1/s | T2/s | |||||||||||
| H-1 | H-2 | H-3 | H-4 | H-5 | H-6 | H-1 | H-2 | H-3 | H-4 | H-5 | H-6 | ||
| 0 | 4.30 | 4.26 | 3.92 | 4.09 | 5.90 | 5.71 | 3.786 | 3.692 | 3.620 | 3.007 | 5.322 | 5.003 | |
| 1 | 1.48 | 1.49 | 1.39 | 1.25 | 1.95 | 1.53 | 0.279 | 0.276 | 0.283 | 0.231 | 0.442 | 0.378 | |
| 3 | 0.59 | 0.58 | 0.56 | 0.48 | 1.09 | 0.81 | 0.092 | 0.090 | 0.094 | 0.080 | 0.212 | 0.188 | |
| 5 | 0.52 | 0.51 | 0.39 | 0.42 | 1.04 | 0.77 | 0.079 | 0.078 | 0.081 | 0.067 | 0.205 | 0.171 | |
| 10 | 0.30 | 0.26 | 0.26 | 0.23 | 0.98 | 0.72 | 0.042 | 0.042 | 0.044 | 0.036 | 0.175 | 0.150 | |
| 15 | 0.15 | 0.08 | 0.08 | 0.09 | 0.85 | 0.63 | 0.018 | 0.021 | 0.022 | 0.016 | 0.127 | 0.119 | |
| 20 | 0.09 | 0.08 | 0.08 | 0.08 | 0.64 | 0.46 | 0.009 | 0.013 | 0.012 | 0.008 | 0.087 | 0.075 | |
| 25 | 0.09 | 0.07 | 0.07 | 0.07 | 0.68 | 0.46 | 0.009 | 0.013 | 0.012 | 0.007 | 0.084 | 0.084 | |
| 30 | 0.09 | 0.07 | 0.07 | 0.07 | 0.68 | 0.46 | 0.009 | 0.012 | 0.012 | 0.007 | 0.083 | 0.081 | |
2.2.3 τc
表2 正丁醇和丙酸质子的τc随HA浓度的变化
Table 2
| CHA/(mg/mL) | τc/ns | |||||
| H-1 | H-2 | H-3 | H-4 | H-5 | H-6 | |
| 0 | 0.13 | 0.13 | 0.11 | 0.18 | 0.12 | 0.13 |
| 1 | 0.88 | 0.89 | 0.83 | 0.89 | 0.76 | 0.70 |
| 3 | 1.00 | 0.94 | 0.96 | 0.96 | 0.85 | 0.74 |
| 5 | 1.02 | 1.00 | 0.96 | 0.99 | 0.85 | 0.77 |
| 10 | 1.08 | 1.00 | 0.96 | 1.00 | 0.91 | 0.81 |
| 15 | 1.19 | 1.00 | 0.96 | 1.00 | 1.04 | 0.88 |
| 20 | 1.32 | 1.00 | 1.00 | 1.32 | 1.10 | 1.00 |
| 25 | 1.32 | 1.00 | 1.00 | 1.32 | 1.17 | 1.00 |
| 30 | 1.32 | 1.00 | 1.00 | 1.32 | 1.18 | 1.00 |
图6
图6
不同HA浓度下,正丁醇、丙酸与HA的结合百分比(ρ).正丁醇和丙酸浓度均为0.5 mg/mL,HA浓度为0~30 mg/mL
Fig.6
The association percentages of HA n-butanol (0.5 mg/mL) and propionic acid (0.5 mg/mL) with different concentrations of HA (0~30 mg/mL)
正丁醇具有线性碳链,具有较强的疏水性,因此能更有效地与HA的疏水结构域相互作用,包裹在HA的疏水区域.而丙酸烷基链较短,与HA的疏水域作用相对于正丁醇弱.丙酸与正丁醇在相同的HA浓度条件下,更容易去质子化,与HA的疏水作用降低,表现出其与HA的结合量要比正丁醇低.
2.2.4 pH值对1H弛豫时间的影响
由于HA富含羧基和酚羟基,因此其与小分子的相互作用、缔合程度受溶液pH值的影响显著.在pH为2~8时(按照1.2.1节中的方式调配)测量了HA存在下(20 mg/mL)的正丁醇H-4的和丙酸H-5的T1(图 7),发现在该pH范围内正丁醇T1值维持在0.10~0.13 s之间,几乎不受溶液pH影响.而丙酸H-5的T1值显著增加,溶液pH=2时,T1为0.42 s;当pH=4,T1增加到0.76 s,并在pH=6时达到最大值0.92 s,而后趋于稳定.可见正丁醇与HA(20 mg/mL)的相互作用不受溶液的pH影响,丙酸与HA(20 mg/mL)相互作用时受溶液pH影响较大,在溶液pH值较低时,有利于丙酸与HA相互作用.有趣的是:我们发现丙酸与不同浓度HA作用时,随着HA浓度的增大,且混合溶液的pH值逐渐增大,丙酸的T1值却逐渐降低,表明丙酸与HA的相互作用逐渐增强.同时,分析图 2可得,HA在20 mg/mL时,丙酸H-5和H-6的耦合裂分明显,表明此时HA与丙酸的相互作用较弱.当HA浓度为30 mg/mL时,H-5和H-6出现明显的宽包,并且在HA浓度逐渐增加时,质子宽包信号变化不明显,说明HA在30 mg/mL时与丙酸的作用达到最大,这表明在HA为20 mg/mL时,丙酸尚未完全包裹在HA疏水区域.随着HA浓度的增加,溶液的pH值逐渐增大,丙酸在溶液pH值较高的状态下,羧基容易去质子化,表现出亲水作用,与HA的作用力较低,但是丙酸与HA之间具有疏水作用且强于其与水之间的亲水作用,所以表现出丙酸与HA的作用力随HA浓度增大而增强.当HA浓度一定时,如20 mg/mL,HA与丙酸之间的疏水作用不变,当调控溶液使其pH增大时,去质子化的丙酸与水的亲水作用力较大,并大于其与HA的疏水相互作用.所以溶液在pH较低时利于丙酸与HA的相互作用.
图7
图7
正丁醇和丙酸的T1与混合溶液pH的关系.正丁醇和丙酸各0.5 mg/mL,HA 20 mg/mL
Fig.7
The pH dependence of the T1 value of n-butanol (0.5 mg/ mL) or propionic acid (0.5 mg/ mL) in the presence of 20 mg/mL HA in D2O
3 结论
本文以正丁醇和丙酸为模型化合物,研究了费托反应生成水与HA的相互作用.结果表明,正丁醇、丙酸与HA之间存在非共价相互作用.在HA(20 mg/mL)存在下,正丁醇和丙酸所有质子的T1平均下降幅度分别为98.5%和90.2%,表明具有疏水特性的HA对正丁醇的相互作用效果比丙酸好.正丁醇与HA作用时被包裹在HA的疏水区域,并且正丁醇与HA作用不受溶液pH的影响.但丙酸与HA作用受溶液pH影响较大,随着HA浓度的增加,溶液pH值逐渐增大,丙酸的羧基容易去质子化,其亲水作用增强,而丙酸与HA之间的疏水作用强于其与水之间的亲水作用,所以表现出丙酸与HA的作用力随HA浓度增大而增强.当HA增加到20 mg/mL,HA与丙酸之间的疏水作用变化不显著,调控溶液使其pH增大,去质子化的丙酸与水的亲水作用力逐渐增大,且作用力大于丙酸与HA的疏水作用,表现为丙酸与HA的作用力降低.因此,HA浓度在0~20 mg/mL,丙酸与HA的疏水作用大于其亲水作用;HA浓度大于20 mg/mL,调控溶液为酸性利于丙酸与HA的相互作用.本研究可为费托反应生成水的处理技术提供基础数据,对于该技术的开发具有指导的意义.
无
参考文献
Application of rectification-pervaporation combined process in the recovery of alcohol products from Fischer-Tropsch waste water
[J].DOI:10.3969/j.issn.1007-6247.2019.03.002 [本文引用: 1]
精馏-渗透汽化联合工艺在费托合成水回收醇类产品中的应用
[J].DOI:10.3969/j.issn.1007-6247.2019.03.002 [本文引用: 1]
Fischer−Tropsch aqueous phase refining by catalytic alcohol dehydration
[J].DOI:10.1021/ie061555r [本文引用: 1]
Utilization of agro-industrial and municipal waste materials as potential adsorbents for water treatment-A review
[J].
Research and application analysis of coal chemical wastewater treatment technology
[J].DOI:10.3969/j.issn.1008-4800.2014.29.240 [本文引用: 1]
煤化工废水处理技术研究及应用分析
[J].DOI:10.3969/j.issn.1008-4800.2014.29.240 [本文引用: 1]
Engineering application of Fischer-Tropsch synthesis wastewater treatment by anaerobic technology
[J].
Fischer-Tropsch acid water processing by Kolbe electrolysis
[J].DOI:10.1016/j.fuel.2017.09.075 [本文引用: 1]
Constructing Fe-based bi-MOFs for photo-catalytic ozonation of organic pollutants in Fischer-Tropsch waste water
[J].DOI:10.1016/j.apsusc.2020.145378
Enhanced degradation of phenolic compounds in coal gasification wastewater by a novel integration of micro-electrolysis with biological reactor (MEBR) under the micro-oxygen condition
[J].DOI:10.1016/j.biortech.2017.12.042 [本文引用: 1]
Catalytic degradation of aqueous Fischer-Tropsch effluents to fuel gas over oxide-supported Ru catalysts and hydrothermal stability of catalysts
[J].DOI:10.1002/jctb.3719 [本文引用: 1]
Structure sensitivity in the ruthenium nanoparticle catalyzed aqueous-phase Fischer-Tropsch reaction
[J].
Ru catalysts supported by Si3N4 for Fischer-Tropsch synthesis
[J].DOI:10.1016/j.apsusc.2020.146631 [本文引用: 1]
A review and experimental verification of using chitosan and its derivatives as adsorbents for selected heavy metals
[J].DOI:10.1016/j.jenvman.2009.10.018 [本文引用: 1]
Applications of chitin- and chitosan-derivatives for the detoxification of water and wastewater-A short review
[J].
Lignite resources and their physical properties in China
[J].
我国褐煤资源及其物性特征
[J].
Highly efficient detoxification of Cr(Ⅵ) by brown coal and kerogen: Process and structure studies
[J].DOI:10.1016/j.fuproc.2016.05.001 [本文引用: 1]
Mechanism study of Cr(Ⅲ) immobilization in the process of Cr(Ⅵ) removal by Huolinhe lignite
[J].DOI:10.1016/j.fuproc.2016.06.037 [本文引用: 1]
The effect of adsorbed chromium on the pyrolysis behavior of brown coal and the recovery of chromium
[J].
Interactions between natural organic matter and organic pollutants as revealed by NMR spectroscopy
[J].DOI:10.1002/mrc.4209 [本文引用: 1]
Solid-state NMR spectroscopic study of phosphate sorption mechanisms on aluminum (hydr)oxides
[J].
The interaction between Fischer-Tropsch wastewater and humic acid: A NMR study of butanol isomers
[J].DOI:10.1016/j.fuproc.2018.07.019 [本文引用: 2]
Micro-organization in dissolved humic acids
[J].DOI:10.1021/es00060a026 [本文引用: 1]
Fluorescence quenching of synthetic organic compounds by humic materials
[J].DOI:10.1021/es00033a012 [本文引用: 1]
Fluorescence lifetime measurements of fluoranthene, 1-naphthol, and napropamide in the presence of dissolved humic acid
[J].DOI:10.1021/es00058a008 [本文引用: 1]
NMR insights into dendrimer-based host-guest systems
[J].DOI:10.1021/cr200333h [本文引用: 1]
Quantum chemical calculation and simulation of Liquid NMR HSQC experiment
[J].
液体核磁共振HSQC实验的量子化学计算与模拟
[J].
Host-guest chemistry and physicochemical properties of the dendrimer-mycophenolic acid complex
[J].
Noncovalent interactions between aromatic compounds and dissolved humic acid examined by nuclear magnetic resonance spectroscopy
[J].
Mechanistic insight into nanoparticle surface adsorption by solution NMR spectroscopy in an aqueous gel
[J].DOI:10.1002/anie.201704471 [本文引用: 1]
A proton nuclear magnetic resonance method for quantitative analysis of ticagrelor
[J].
定量核磁共振氢谱测定新药替格瑞洛
[J].
Direct determination of NMR correlation times from spin-lattice and spin-spin relaxation times
[J].DOI:10.1021/jp963338h [本文引用: 1]
Direct-determination of 15N- and 19F-NMR correlation times from spin-lattice and spin-spin relaxation times
[J].DOI:10.1021/jp9720799 [本文引用: 1]
Noncovalent interactions between aromatic compounds and dissolved humic acid examined by nuclear magnetic resonance spectroscopy
[J].
1H NMR explores the influence of steric effect on the synergistic effect of surfactant compound system
[J].
1H NMR探究空间效应对表面活性剂复配体系中协同作用的影响
[J].
NMR study on the interaction between PAMAM dendrimer and 5-fluorouracil
[J].
PAMAM树状大分子与5-氟尿嘧啶相互作用的NMR研究
[J].
Ternary deep eutectic solvents catalyzed d-glucosamine self-condensation to deoxyfructosazine: NMR study
[J].DOI:10.1016/j.gee.2020.04.010 [本文引用: 1]
Noncovalent interactions between acenaphthenone and dissolved fulvic acid as determined by 13C NMR T1 relaxation measurements
[J].DOI:10.1021/es960391a [本文引用: 2]
Quantitative evaluation of noncovalent interactions between glyphosate and dissolved humic substances by NMR spectroscopy
[J].DOI:10.1021/es300265a [本文引用: 1]
Host-guest interactions between 2, 4-dichlorophenol and humic substances as evaluated by 1H NMR relaxation and diffusion ordered spectroscopy
[J].
Binding of phenol and differently halogenated phenols to dissolved humic matter as measured by NMR spectroscopy
[J].DOI:10.1021/es900559b [本文引用: 1]