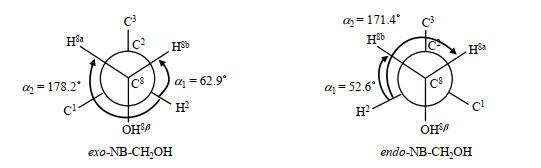引言
降冰片烯(Norbornene,NB)及其衍生物具备合适的环张力和便于衍生化[1]等优点,是聚合反应中用于新型催化剂筛选和新型聚降冰片烯基高分子制备的重要单体,在工程塑料、生物材料和光学材料等领域被广泛应用[2].降冰片烯及其衍生物一般是由环戊二烯与乙烯或乙烯基衍生物通过Diels-Alder反应制备,但是该方法制备的降冰片烯衍生物为内型和外型异构体的混合物,且由于过渡态的位阻效应和次级HOMO-LUMO轨道相互作用的影响,所得产物以内型为主[3].在内型降冰片烯衍生物中,由于取代基与双键位置邻近,阻碍了开环易位聚合反应中过渡金属催化剂与双键接近引起的金属四元环过渡态的形成,表现出相较于外型单体较慢的聚合反应速率[4].但是,到目前为止,在商品化的降冰片烯单取代衍生物中,仅有外型-5-降冰片烯-2-羧酸((1R, 2S, 4R)-二环[2.2.1]庚-5-烯-2-羧酸)是单一构型结构,其余均为内型占优(一般80%以上)的内型和外型结构的混合物,如5-降冰片烯-2-羧酸、5-降冰片烯-2-甲醇和5-降冰片烯-2-甲胺等.由于降冰片烯环的各向异性效应使环上同碳质子为磁不等价质子,加之又存在外型和内型两种构型异构体,因此其核磁共振(NMR)谱图复杂,导致基于降冰片烯衍生物所制备的新化合物的结构确认非常困难.据我们所知,目前文献[5-10]仅对它们的1H NMR信号进行简单的分类,但是其完整的波谱学数据,以及1H和13C NMR信号的完全归属还未见报道.
5-降冰片烯-2-羧酸和5-降冰片烯-2-甲醇是降冰片烯衍生化的两类重要前体,在本文作者所在实验室制备的外消旋化的单一构型5-降冰片烯-2-羧酸和5-降冰片烯-2-甲醇的基础上,本文利用1H NMR、DEPT135、1H-1H COSY、1H-13C HMQC、1H-1H NOESY谱和相应的耦合裂分信息,对外型-5-降冰片烯-2-羧酸(exo-5-norbornene-2-carboxylic acid,exo-NB-COOH)、内型-5-降冰片烯-2-羧酸(endo-5- norbornene-2-carboxylic acid,endo-NB-COOH)、外型-5-降冰片烯-2-甲醇(exo-5-norbornene-2- methanol,exo-NB-CH2OH)和内型-5-降冰片烯-2-甲醇(endo-5-norbornene-2-methanol,endo-NB- CH2OH)的1H和13C NMR信号进行归属,并探讨了降冰片烯衍生物的取代基种类及空间构型对1H NMR化学位移的影响.这将对所制备的新的降冰片烯衍生物的结构鉴定提供重要依据.
1 实验部分
exo-NB-COOH、endo-NB-COOH、exo-NB-CH2OH和endo-NB-CH2OH均为实验室制备,其合成方法另文报道,其能量最低构象用Chem3D软件里的MM2分子力场方法进行能量优化.氘代氯仿(CDCl3,氘代率大于99.9%)购自剑桥同位素实验室公司,含0.03 v %的四甲基硅烷(TMS).
NMR数据采集在Agilent 600 MHz NMR波谱仪上进行,1H和13C NMR的工作频率分别为599.60 MHz和150.77 Hz.1H NMR谱宽为16 ppm(δH −2~14),13C NMR谱宽为250 ppm(δC −15~235),温度为25℃,以TMS中的甲基信号进行定标(δH 0.00、δC 0).DEPT135谱宽为250 ppm,扫描次数为128;2D NMR(1H-1H COSY、1H-13C HMQC和1H-1H NOESY)实验均采用标准脉冲序列.1H-13C HMQC的F2(1H)和F1(13C)维谱宽分别为16 ppm和170 ppm,采样数据点阵为t2×t1=4 096×2 048;1H-1H COSY的F2(1H)和F1(1H)维谱宽均为9.5 ppm,采集数据点阵为t2×t1= 2 048×2 048;1H-1H NOESY的F2(1H)和F1(1H)维谱宽均为12.5 ppm,混合时间为0.6 s,采样数据点阵为t2×t1=4 096×4 096.
2 结果与讨论
2.1 降冰片烯衍生物的化学结构及能量最低构象
exo-NB-COOH、endo-NB-COOH、exo-NB-CH2OH和endo-NB-CH2OH的化学结构和碳、氢原子编号,以及计算机模拟能量最低构象如图 1所示.
图1
图1
(a) exo-NB-COOH、(b) endo-NB-COOH、(c) exo-NB-CH2OH和(d) endo-NB-CH2OH的化学结构及计算机模拟能量最低构象(碳原子:灰色;氢原子:紫色;氧原子:红色)
Fig.1
The chemical structures of (a) exo-NB-COOH, (b) endo-NB-COOH, (c) exo-NB-CH2OH, and (d) endo-NB-CH2OH, and their calculated conformations with minimum energy (the gray, purple, and red balls stand for the C, H, and O atoms, respectively)
2.2 降冰片烯衍生物的NMR谱图及其归属
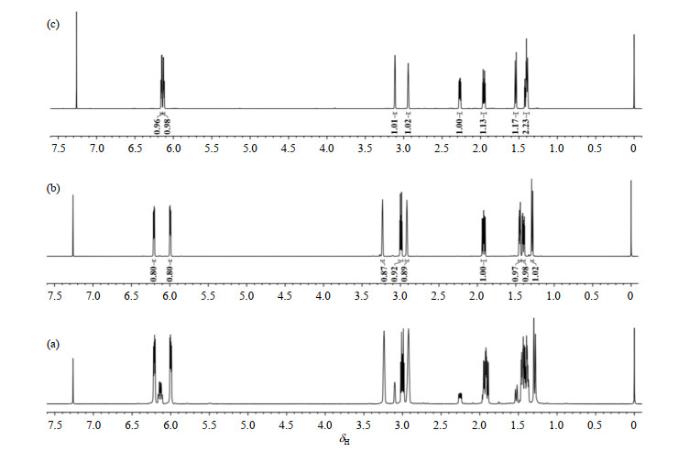
一般来说,对于结构简单的化合物,我们可结合质子在化合物中所处的化学环境,根据化学位移、耦合常数和积分面积等信息,通过1H NMR谱图就可以对相应的质子进行归属,进而推断化合物的结构[11].但是由于降冰片烯环的各向异性效应,且其常见的C-2位单取代衍生物又存在外型(exo)和内型(endo)两种异构体,致使其一维1H NMR谱图非常复杂,如存在谱峰重叠和多重耦合等,难以对其质子进行准确归属.图 2(a)是市售的内型占优的NB-COOH(购自Alfa Aesar,97%)的1H NMR谱图,我们只能判断其烯烃质子位于δH 5.99~6.22之间;根据烯烃质子的积分面积计算其endo-NB-COOH和exo-NB-COOH的摩尔比大致为4:1;另外根据化学位移以及谱峰的分组情况,大致可判断桥头氢H-1和H-4位于δH 2.93~3.24,但无法对其具体位置进行准确归属;而降冰片烯环上的其它质子,如H-2、H-3a、H-3b、H-7a、H-7b等,则难以归属.尽管单一构型的降冰片烯羧酸排除了构型异构体的干扰,1H NMR谱图[图 2(b)和图 2(c)]清晰易分辨,但是其降冰片烯环上的质子仍然难以准确归属.这为基于该结构的降冰片烯衍生物的1H NMR谱图分析带来困难.
图2
图2
(a) NB-COOH(外型和内型混合物,内型占优)、(b) endo-NB-COOH和(c) exo-NB-COOH的1H NMR谱图
Fig.2
1H NMR spectra of (a) NB-COOH (mixture of endo and exo, predominantly endo isomer), (b) endo-NB-COOH, and (c) exo-NB-COOH
2.2.1 exo-NB-COOH的结构解析
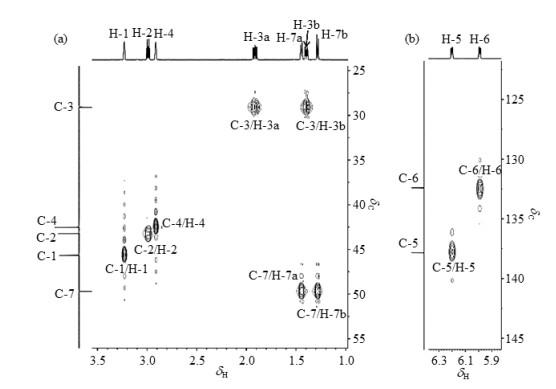
由exo-NB-COOH的1H NMR谱图[图 2(c)]并结合化学位移规律,可以看出,δH 6.12和δH 6.15归属为与C=C双键相连的质子H-5和H-6,但两者的具体归属暂时无法确认.至于降冰片烯环上其它质子的归属,仅从1H NMR谱图中无法得出准确结论.因此,我们进一步通过DEPT135谱(图S1,可扫描首页OSID码,或在论文网页版查看)确定了两个仲碳原子C-3/C-7的化学位移为δC 30.3/46.4,但二者的具体位置也无法确认.1H-13C HMQC谱(图 3)显示,δH 1.40、1.96与δC 30.3相关;δH 1.39、δH 1.54和δC 46.4相关.此外,我们根据δH 2.94和3.11的峰形(多重耦合,近似宽的单峰),推测其为桥头氢H-1和H-4.1H-13C HMQC谱显示,δH 2.94与δC 41.7相关;δH 3.11与δC 46.7相关,推断两个桥头碳原子C-1/C-4为δC 41.7/46.7,但两者的具体位置也暂时无法确认.1H NMR谱中余下的δH 2.27归属为与C-2相连的H-2,表现为多重峰,证明其与多个质子存在耦合关系;再根据1H-13C HMQC谱,将δC 43.1归属为C-2.
图3
图3
exo-NB-COOH的局部1H-13C HMQC谱图
Fig.3
Partial 1H-13C HMQC spectrum of exo-NB-COOH
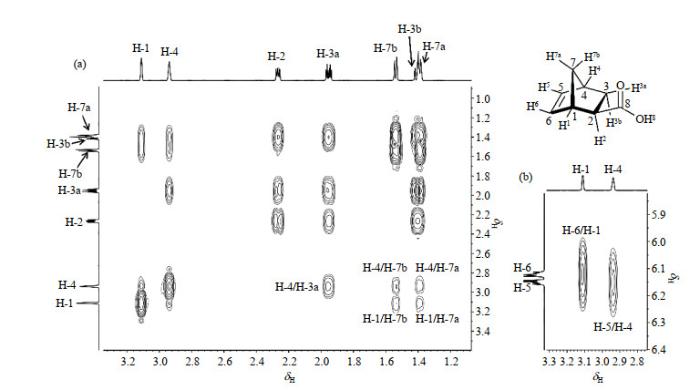
我们又进一步分析了exo-NB-COOH的1H-1H COSY谱,希望通过氢核之间的耦合情况对各组质子进行准确归属.从图 4(a)中可以看出,两个桥头氢原子H-1和H-4与δH 1.39和δH 1.54耦合强度相同,说明δH 1.39和δH 1.54属于H-7a和H-7b,但二者的具体位置暂时无法确认;则δH 1.40/1.96为H-3a或H-3b. δH 2.94(H-1或H-4)与δH 1.96(H-3a或H-3b)存在较强的耦合,而与H-2(δH 2.27)和δH 1.40(H-3a或H-3b)耦合强度很弱或不存在耦合.我们结合exo-NB-COOH的优势构象,分别计算出H-1−C-1−C-2−H-2所形成的二面角α为81.7˚;H-4−C-4−C-3−H-3a和H-4−C-4−C-3−H-3b所形成的二面角α1和α2分别为43.3˚和77.3˚(图 5).根据Karplus关系[14],当二面角α在0˚~90˚区间时,耦合强度随着α的增加而减小,在90˚时耦合强度最小;当二面角α在90˚~180˚区间时,耦合强度随着α的增加而增加,在90˚时耦合强度最小,180˚时耦合强度最大.因此,我们推测δH 2.94与δH 1.96的耦合关系应为H-4与H-3a之间的耦合,δH 2.94和δH 1.96分别归属为H-4和H-3a.结合上述分析,δH 3.11归属为H-1;δH 1.40归属为H-3b.另外,依据桥头氢H-1和H-4与双键上质子的耦合关系[图 4(b)],将δH 6.12和δH 6.15分别归属为H-6和H-5.
图4
图5
图5
exo-NB-COOH中C-2−C-1和C-4−C-3构象的Newman投影式
Fig.5
Depict the conformations of C-2−C-1 and C-4−C-3 of exo-NB-COOH in a Newman projection
至此,仅剩下H-7a和H-7b未归属.我们又从exo-NB-COOH的1H-1H NOESY谱(图 6)中可以看出,δH 1.39与δH 6.12、δH 6.15出现交叉峰,说明此氢原子与H-5、H-6在空间上距离比较近.结合exo-NB-COOH的空间构型,我们把δH 1.39归属为与双键在桥环同侧的质子H-7a,这样也就确定了H-7b的化学位移为δH 1.54.此外,从NOESY谱还可以观察到δH 1.96(H-3a)与δH 1.54(H-7b)的交叉峰,也进一步验证我们推断的正确性.
图6
图6
exo-NB-COOH的局部1H-1H NOESY谱图
Fig.6
Partial 1H-1H NOESY spectrum of exo-NB-COOH
在确定exo-NB-COOH所有质子的化学位移之后,可以很容易地从1H-13C HMQC谱图中归属出降冰片烯环上相应碳原子的化学位移,而DEPT135 NMR谱图中不显示的季碳(C-8)化学位移可以从常规13C NMR谱图获得(图S1).exo-NB-COOH的1H和13C NMR归属见表 1.
表1 exo-NB-COOH上的1H和13C NMR化学位移归属
Table 1
| Position | δC | δH (J/Hz) | 1H-1H COSY | 1H-13C HMQC |
| 1 | 46.7 | 3.11 (1H, m) | H-6, 7a, 7b | + |
| 2 | 43.1 | 2.27 (1H, m) | H-3a, 3b | + |
| 3a b | 30.3 | 1.96 (1H, dt, J1=11.4 Hz, J2=3.0 Hz) 1.40 (1H, m) | H-2, 3b, 4 H-2, 3a, 4 | + |
| 4 | 41.7 | 2.94 (1H, m) | H-3a, 3b, 5, 7a, 7b | + |
| 5 | 138.1 | 6.15 (1H, dd, J1=5.4 Hz, J2=3.0 Hz) | H-4, 6 | + |
| 6 | 135.7 | 6.12 (1H, dd, J1=5.4 Hz, J2=3.0 Hz) | H-1, 5 | + |
| 7a b | 46.4 | 1.39 (1H, d, J=8.4 Hz) 1.54 (1H, d, J=8.4 Hz) | H-1, 4, 7b H-1, 4, 7a | + |
| 8 | 182.7 | 11.61 (1H, br) | / | / |
2.2.2 endo-NB-COOH的结构解析
endo-NB-COOH的谱图解析过程与exo-NB-COOH类似.由endo-NB-COOH的1H NMR谱图[图 2(b)],并结合质子化学位移的规律可以看出,δH 6.00和δH 6.21归属为与C=C双键相连的质子H-5和H-6,但两者的具体位置暂时无法确认.至于降冰片烯环上其它质子的归属,仅从1H NMR谱图中无法得出准确结论.因此,我们进一步通过DEPT135谱(图S2)确定了两个仲碳原子C-3/C-7的化学位移为δC 29.1/49.7,但二者的具体位置也暂时无法确认.1H-13C HMQC谱(图 7)显示,δH 1.40、1.92与δC 29.1相关;δH 1.29、δH 1.45和δC 49.7相关.此外,我们根据δH 2.92和3.23的峰形(多重耦合,近似宽的单峰),推测其为桥头氢H-1和H-4.1H-13C HMQC谱显示,δH 2.92与δC 42.5相关;δH 3.23与δC 45.7相关,推断两个桥头碳原子C-1/C-4为δC 42.5/45.7,但两者的具体位置也暂时无法确认.1H NMR谱中余下的δH 3.00归属为与C-2相连的H-2,表现为多重峰,证明其与多个质子存在耦合关系;根据1H-13C HMQC谱,将δC 43.2归属为C-2.
图7
图7
endo-NB-COOH的局部1H-13C HMQC谱图
Fig.7
Partial 1H-13C HMQC spectra of endo-NB-COOH
在确定H-2的化学位移之后,可进一步通过1H-1H COSY谱[图 8(a)]确定与H-2存在耦合关系的桥头氢原子H-1为δH 3.23,则δH 2.92归属为H-4.通过H-1和H-4与双键氢原子的耦合关系,我们进一步确定H-6和H-5的化学位移分别为δH 6.00和δH 6.21.另外,在降冰片烯环顶端两个质子H-7a和H-7b的推断中,由1H-1H NOESY谱(图S3)可以看出,δH 1.45与δH 6.00、δH 6.21出现交叉峰,说明此氢原子与H-5、H-6在空间上距离比较近.结合endo-NB-COOH的空间构型,我们把δH 1.45归属为与双键在桥环同侧的质子H-7a,同时也就确定了δH 1.29归属为H-7b.此外,从NOESY谱还可以观察到δH 1.92(H-3a)和δH 3.00(H-2)与δH 1.29(H-7b)的交叉峰,也佐证了我们归属的正确性.
图8
图8
endo-NB-COOH的(a)局部1H-1H COSY谱图和(b) 1H NMR谱图
Fig.8
Partial (a) 1H-1H COSY and (b) 1H NMR spectra of endo-NB-COOH
H-3a和H-3b的归属可以通过二者与H-2的耦合强度加以区分.从图 8(a)可以看出,H-2(δH 3.00)与δH 1.92的耦合信号明显强于与δH 1.40的耦合.结合endo-NB-COOH的优势构象[图 1(b)],H-2−C-2−C-3−H-3a和H-2−C-2−C-3−H-3b的二面角分别为2.8˚和125.2˚,根据Karplus关系[14],H-2和H-3a有较强的耦合作用.因此,将δH 1.92和δH 1.40分别归属为H-3a和H-3b.除1H-1H COSY谱图外,我们也可对1H NMR谱中耦合常数加以分析.如图 8(b)所示,H-2(δH 3.00)呈现为dt峰.但根据耦合规律,理论上H-2应为ddd峰,因耦合常数相同,简并为dt峰,其三组耦合常数分别J1 (H-2/H-3a) = 9.6 Hz,J2 (H-2/H-1) = J3 (H-2/H-3b) = 4.2 Hz;H-3a为ddd耦合,表现为八重峰,其三组耦合常数分别为J1 (H-3a/H-3b) =12.0 Hz,J2 (H-3a/H-2) = 9.0 Hz,J3 (H-3a/H-4) = 3.6 Hz;H-3b也为ddd耦合,表现为八重峰,其三组耦合常数分别为J1 (H-3b/H-3a) = 12.0 Hz,J2 (H-3b/H-2) = 4.2 Hz,J3 (H-3b/H-4) = 2.4 Hz.H-3a和H-3b间的耦合常数最大(J=12.0 Hz),为二者之间的同碳2J耦合.结合H-2、H-3a和H-3b的空间构型,H-2与H-3a在降冰片烯环的同侧,二者与C-2、C-3所形成的二面角为2.8˚,存在一个较强的邻位3J耦合,耦合常数约为9.0 Hz;而H-2与H-3b位于降冰片烯环的不同侧,耦合常数较小,仅为4.2 Hz.因此,耦合常数的分析可以进一步佐证由1H-1H COSY谱图得到的质子归属的正确性.
在确定endo-NB-COOH所有质子的化学位移之后,可以方便地从1H-13C HMQC谱中归属出降冰片烯环上碳原子的化学位移,而DEPT135谱图中不显示的季碳(C-8)化学位移可以从常规13C NMR谱图获得(13C NMR和DEPT135谱见图S2).endo-NB-COOH的1H和13C NMR谱峰信息及相应归属见表 2.
表2 endo-NB-COOH上的1H和13CNMR化学位移归属
Table 2
| Position | δC | δH (J/Hz) | 1H -1H COSY | 1H-13C HMQC |
| 1 | 45.7 | 3.23 (1H, m) | H-2, 6, 7a, 7b | + |
| 2 | 43.2 | 3.00 (1H, dt, J1=9.6 Hz, J2=J3=4.2 Hz) | H-1, 3a, 3b | + |
| 3a b | 29.1 | 1.92 (1H, ddd, J1=12.0 Hz, J2=9.0 Hz, J3=3.6 Hz) 1.40 (1H, ddd, J1=12.0 Hz, J2=4.2 Hz, J3=2.4 Hz) | H-2, 3b, 4 H-2, 3a, 4 | + |
| 4 | 42.5 | 2.92 (1H, m) | H-3a, 3b, 5, 7a, 7b | + |
| 5 | 137.9 | 6.21 (1H, dd, J1=6.0 Hz, J2=3.0 Hz) | H-4, 6 | + |
| 6 | 132.5 | 6.00 (1H, dd, J1=6.0 Hz, J2=3.0 Hz) | H-1, 5 | + |
| 7a b | 49.7 | 1.45 (1H, ddd, J1=8.4 Hz, J2=4.2 Hz, J3=2.4 Hz) 1.29 (1H, d, J=8.4 Hz) | H-1, 4, 7b H-1, 4, 7a | + |
| 8 | 181.1 | 11.29 (1H, br) | / | / |
2.2.3 exo-NB-CH2OH的结构解析
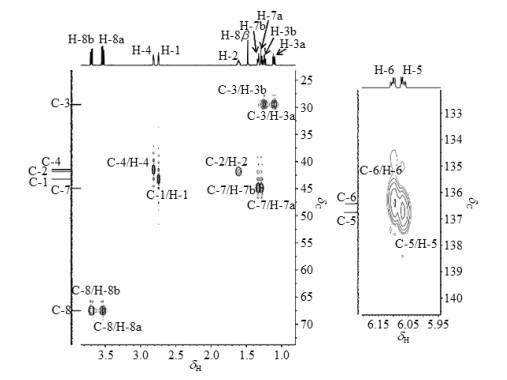
对于exo-NB-CH2OH谱图的解析,首先由1H NMR谱图(图S4),并结合质子化学位移的规律,δH 6.07和δH 6.11归属为与C=C双键相连的质子H-5和H-6,但两者的具体位置暂时无法确认.δH 3.53和δH 3.70归属为与羟基相连的质子H-8a和H-8b,两者的具体位置暂时无法确认.δH 1.49(单峰)归属为羟基质子H-8β.从exo-NB-CH2OH的1H-13C HMQC谱(图 9)可以看出,δH 1.11和1.25与δC 29.5相关;δH 1.29和δH 1.34与δC 44.9相关,δH 3.53和δH 3.70与δC 67.5相关.我们根据δH 2.75和2.82的峰形(多重耦合,近似宽的单峰),推测其为桥头氢H-1和H-4,但具体位置也是暂时无法确认.另外,再根据1H-13C HMQC谱的交叉峰,δH 2.75与δC 43.3相关;δH 2.82与δC 41.5相关,推断两个桥头碳原子C-1/C-4为δC 43.3/41.5,但两者的具体位置也暂时无法确认.1H NMR谱中剩余的δH 1.62归属为与C-2相连的H-2,表现为多重峰,证明其与多个质子存在耦合关系.H-2化学位移小于exo-NB-COOH中相应质子(δH 2.27),这主要归因于羟甲基的吸电子诱导效应弱于羧基[15].
图9
图9
exo-NB-CH2OH的局部1H-13C HMQC谱图
Fig.9
Partial 1H-13C HMQC spectra of exo-NB-CH2OH
与exo-NB-COOH的分析类似,位于exo位置的质子H-3a与桥头氢原子H-4存在较强的耦合[图 10(a)],因此,可以确定H-3a为δH 1.11(1H,dt,J1=12.0 Hz,J2=J3=4.2 Hz);H-3b则为δH 1.25(1H,ddd,J1=12.0 Hz,J2=8.4 Hz,J3=2.4 Hz)、H-4为δH 2.82(1H,m)、H-1为δH 2.75(1H,m).从桥头氢原子与双键质子之间的耦合关系[图 10(b)],我们又可以确定H-5和H-6分别为δH 6.07和δH 6.11. 另外,在归属H-7a和H-7b时,我们根据exo-NB-COOH的NOESY谱的归属规律,分别将δH 1.29归属为H-7a,δH 1.34归属为H-7b.
图10
图10
exo-NB-CH2OH的(a, b)局部1H-1H COSY谱图和(c)1H NMR谱图
Fig.10
Partial (a, b) 1H-1H COSY spectra and (c) 1H NMR spectra of exo-NB-CH2OH
由于C-8与降冰片烯环上的手性碳原子C-2相连,因此与C-8相连的H-8a和H-8b是化学不等价的,表现出不同的化学位移.对于H-8a和H-8b的准确判断,难以通过化学位移或1H-1H COSY谱中与其它质子的相互耦合得到有效信息;但是我们可借助H-8a和H-8b与H-2的3J耦合常数,以及H-2−C-2−C-8−H-8a(H-8b)所组成的二面角α,通过Karplus关系[14]加以判断.结合图 1中所模拟出的exo-NB-CH2OH优势空间构象,如图 11所示,H-2−C-2−C-8−H-8b的二面角α1=62.9˚,而与H-2−C-2−C-8−H-8a的二面角α2=178.2˚,因此H-2与H-8a间的耦合作用要强于H-2与H-8b之间的耦合.位于δH 3.53处的dd峰的两个耦合常数分别为10.8 Hz和8.4 Hz,而位于δH 3.70处的dd峰的两个耦合常数分别为10.8 Hz和6.6 Hz.其中,最大的耦合常数(J=10.8 Hz)是来自H-8a和H-8b之间的2J耦合,而相对较小的耦合则为H-8a(H-8b)与H-2之间的3J耦合.因此,H-8a和H-8b分别为δH 3.53(1H,dd,J1=10.8 Hz,J2=8.4 Hz)和δH 3.70(1H,dd,J1=10.8 Hz,J2=6.6 Hz).
图11
图11
exo-NB-CH2OH和endo-NB-CH2OH中C-2−C-8构象的Newman投影式
Fig.11
Depict the conformations of C-2−C-8 of exo-NB-CH2OH and endo-NB-CH2OH in a Newman projection
羟基质子易与溶剂中的质子间的快速交换常使其不与其相邻碳氢耦合而表现出单峰.因此,根据峰形,粗略确定羟基上的质子为δH 1.49.需要指出的是,由于羟基氢为活泼氢,它的化学位移与样品的浓度、温度以及微量水的存在等因素均有关系,其化学位移并不固定.我们在体系中额外加入2滴重水(D2O)后,δH 1.49处的信号由于存在重氢交换而消失(图S5),这进一步确认其为羟基质子的信号峰.
在确定exo-NB-CH2OH所有质子的化学位移之后,可以很容易地从1H-13C HMQC谱图中归属出降冰片烯环上碳原子的化学位移(13C NMR和DEPT135 NMR谱见图S6).exo-NB-CH2OH的1H和13C NMR归属见表 3.
表3 exo-NB-CH2OH上的1H和13CNMR化学位移归属
Table 3
| Position | δC | δH (J/Hz) | 1H -1H COSY | 1H-13C HMQC |
| 1 | 43.3 | 2.75 (1H, m) | H-6, 7a, 7b | + |
| 2 | 41.9 | 1.62 (1H, m) | H-3a, 3b, 8a, 8b | + |
| 3a b | 29.5 | 1.11 (1H, dt, J1=12.0 Hz, J2=J3=4.2 Hz) 1.25 (1H, ddd, J1=12.0 Hz, J2=8.4 Hz, J3=2.4 Hz) | H-2, 3b, 4 H-2, 3a, 4 | + |
| 4 | 41.5 | 2.82 (1H, m) | H-3a, 3b, 5, 7a, 7b | + |
| 5 | 136.8 | 6.07 (1H, dd, J1=6.0 Hz, J2=3.0 Hz) | H-4, 6 | + |
| 6 | 136.4 | 6.11 (1H, dd, J1=6.0 Hz, J2=3.0 Hz) | H-1, 5 | + |
| 7a b | 44.9 | 1.29 (1H, d, J1=9.0 Hz) 1.34 (1H, d-quint, J1=9.0 Hz, J2=1.8 Hz) | H-1, 4, 7b H-1, 4, 7a | + |
| 8a b 8β | 67.5 | 3.53 (1H, dd, J1=10.8 Hz, J2=8.4 Hz) 3.70 (1H, dd, J1=10.8 Hz, J2=6.6 Hz) 1.49 (1H, s) | H-2, 8b H-2, 8a / | + |
2.2.4 endo-NB-CH2OH的结构解析
结合endo-NB-COOH和exo-NB-CH2OH NMR谱图的解析方法,对endo-NB-CH2OH中的1H和13C NMR进行了归属.但由于篇幅关系,解析过程就不再赘述. endo-NB-COOH的1H NMR、13C NMR、DEPT135、1H-13C HMQC和1H-1H COSY谱见图S7~S10,1H和13C NMR谱峰归属见表 4.
表4 endo-NB-CH2OH上的1H和13C化学位移归属
Table 4
| Position | δC | δH (J/Hz) | 1H -1H COSY | 1H-13C HMQC |
| 1 | 43.6 | 2.93 (1H, m) | H-2, 6, 7a, 7b | + |
| 2 | 41.7 | 2.29 (1H, m) | H-1, 3a, 3b, 8a, 8b | + |
| 3a b | 28.8 | 1.82 (1H, ddd, J1=12.0 Hz, J2=9.0 Hz, J3=3.6 Hz) 0.52 (1H, ddd, J1=12.0 Hz, J2=4.2 Hz, J3=2.4 Hz) | H-2, 3b, 4 H-2, 3a, 4 | + |
| 4 | 42.2 | 2.81 (1H, m) | H-3a, 3b, 5, 7a, 7b | + |
| 5 | 137.4 | 6.14 (1H, dd, J1=6.0 Hz, J2=3.0 Hz) | H-4, 6 | + |
| 6 | 132.1 | 5.95 (1H, dd, J1=6.0 Hz, J2=3.0 Hz) | H-1, 5 | + |
| 7a b | 49.5 | 1.45 (1H, dm, J1=8.4 Hz) 1.27 (1H, d, J1=8.4 Hz) | H-1, 4, 7b H-1, 4, 7a | + |
| 8a b 8β | 66.5 | 3.26 (1H, dd, J1=10.2 Hz, J2=8.4 Hz) 3.40 (1H, dd, J1=10.2 Hz, J2=6.6 Hz) 1.42 (1H, s) | H-2, 8b H-2, 8a / | + |
2.3 内型和外型降冰片烯衍生物的1H化学位移比较
2.3.1 exo-NB-COOH和endo-NB-COOH的1H化学位移比较
我们进一步对exo-NB-COOH和endo-NB-COOH的1H化学位移进行了比较研究.由表 1和表 2可以看出,exo-NB-COOH和endo-NB-COOH中的1H的化学位移差别最大的为H-2,endo-NB-COOH的H-2较exo-NB-COOH向低场移动了0.73 ppm,我们认为其主要原因在于在endo-NB-COOH中,H-2位于羰基(C=O)的去屏蔽区,使化学位移向低场移动.另外,对于exo-NB-COOH的H-7b,其化学位移相较于endo-NB-COOH向低场移动了0.25 ppm,我们认为在exo-NB-COOH的空间结构中由于H-7b位于羰基(C=O)的去屏蔽区所致.另外,在exo-NB-COOH中,双键上的质子H-5和H-6的化学位移相近,说明当羧基处在外型位置时,对降冰片烯环的构象影响较小;但是当羧基处于内型位置时(endo-NB-COOH),H-6明显地移向高场,H-5与H-6的化学位移存在0.21 ppm的差值(而这一数值在exo-NB-COOH中仅为0.03 ppm),推测其主要原因为当羧基处于C-2的内型位置时,羧基与降冰片烯环中C-1、C-4、C-5、C-6所组成的平面具有较大排斥作用,致使整个降冰片烯环可能会发生一定程度的扭曲,进而引起H-5与H-6出现一定的化学环境差异,表现出较为明显的化学位移差别.
2.3.2 exo-NB-CH2OH和endo-NB-CH2OH的1H化学位移比较
在对endo-NB-CH2OH的1H化学位移进行归属后,我们发现H-3b的化学位移处于一个非常高场的位置,达到δH 0.52,而这种现象并没有在相应的endo-NB-COOH中观察到.我们推测这可能是由于在endo-NB-CH2OH结构中,降冰片烯环可能存在一定的扭曲,使H-3b处在C-5和C-6双键的屏蔽区,使化学位移向高场移动.需要指出的是,在其它三个结构(exo-NB-COOH,endo-NB-COOH和exo-NB-CH2OH)中,均没有观察到H-3b的化学位移明显地移向高场.另一方面,C-8上体积较大的羟甲基的范德华(van der Waals)效应也可能是使H-3b化学位移移向高场的另一影响因素[15].
3 结论
本文综合运用1H NMR、13C NMR、DEPT135、1H-1H COSY、1H-13C HMQC和1H-1H NOESY谱图和相应的耦合裂分信息,对exo-NB-COOH、endo-NB-COOH、exo-NB-CH2OH和endo-NB-CH2OH的1H和13C NMR信号进行了归属.在此基础上,讨论了降冰片烯衍生物的取代基种类及空间构型对1H NMR化学位移的影响.该研究为基于降冰片烯衍生物的空间结构解析提供重要依据.
附件材料
图S1 exo-NB-COOH的13C NMR和DEPT135谱图
图S2 endo-NB-COOH的13C NMR和DEPT135谱图
图S3 endo-NB-COOH的1H-1H NOESY NMR谱图
图S4 exo-NB-CH2OH的1H NMR谱图
图S5 (a) exo-NB-CH2OH的1H NMR谱图;(b) 向体系中加入2滴D2O后的1H NMR谱图
图S6 exo-NB-CH2OH的13C NMR和DEPT135谱图
图S7 endo-NB-CH2OH的1H NMR谱图
图S8 endo-NB-CH2OH的13C NMR和DEPT135谱图
图S9 endo-NB-CH2OH的局部1H-13C HMQC谱图
图S10 endo-NB-CH2OH的局部1H-1H COSY谱图
无
参考文献
Evaluation of strain in hydrocarbons. The strain in adamantane and its origin
[J].DOI:10.1021/ja00711a030 [本文引用: 2]
Ring-opening metathesis polymerisation derived poly(dicyclopentadiene) based materials
[J].DOI:10.1039/D0QM00296H [本文引用: 3]
Origin of the "Endo Rule" in Diels-Alder reactions
[J].DOI:10.1002/jcc.23500 [本文引用: 1]
ROMP reactivity of endo- and exo-dicyclopentadiene
[J].DOI:10.1021/ma0209489 [本文引用: 1]
The Synthesis and absolute configuration of optically active tricyclo[4.3.0.03, 8] nonane (Twist-brendane)
[J].DOI:10.1246/bcsj.46.888 [本文引用: 1]
Enzymatic resolution of norbor(NE)nylmethanols in organic media and an application to the synthesis of (+)- and (−)-endo-norbornene lactone
[J].DOI:10.1016/S0040-4020(01)80984-4
Synthesis of chiral sultams and their application as chiral auxiliaries in an asymmetric Diels-Alder reaction
[J].DOI:10.1016/j.tetasy.2004.12.026
More than a protective group: Synthesis and applications of a new chiral silane
[J].
Stereo-selective synthesis of exo-norbornene derivatives for resist materials
[J].DOI:10.2494/photopolymer.22.365
Stereo-selective synthesis of 5-Norbornene-2-exo-carboxylic scid-rapid isomerization and kinetically selectivehydrolysis
[J].DOI:10.4236/ijoc.2012.21005 [本文引用: 1]
Structural assignment and quantitative analysis for hydrogenation products of anthracene by NMR technology
[J].DOI:10.11938/cjmr20202849 [本文引用: 1]
蒽加氢产物的结构指认和定量核磁共振分析
[J].DOI:10.11938/cjmr20202849 [本文引用: 1]
An NMR analysis of 10-indol cytochalasin chaetoglobosin F
[J].
10-吲哚细胞松弛素chaetoglobosin F的NMR解析
[J].
Vicinal proton coupling in nuclear magnetic resonance
[J].DOI:10.1021/ja00901a059 [本文引用: 3]