引言
当前新能源产业蓬勃兴起,动力电池成为产业核心技术之一,其技术水平直接关系到产业的未来发展.锂离子电池作为动力电池主流,已在电动车、手机、电脑、汽车和航空等多个领域得到拓展和应用.锂离子电池的快速发展和应用使得其电解质材料的研究也面临越来越多的挑战[1],近年来电解质材料研究虽然取得了诸多重大突破[2-4],但是兼顾高电导率、高安全性、抗氧化性和经济性的材料仍非常少见.有机硅化合物是一类具有许多特殊性质的新型材料,由于其具有优良的热稳定性和低温离子传导性能、高电导率、低可燃性和高分解电压等优势,已成为电解质材料研究的关注热点[5].有机硅化合物作为锂盐溶剂代替传统电解液或作为添加剂表现出优良性能[6, 7],可提高电池安全性和导电性、使用寿命等相关特性.此外,其燃烧时释放低毒气体,具有显著的环境友好性[8].
电解质材料物理特性是衡量电池性能的重要参数,直接影响电池的性能和使用效果.如热稳定性能影响使用寿命,扩散系数影响导电能力,溶剂效应则影响电池超级电容电化学性能[9].目前,国内外用来研究电解质材料热稳定性的方法主要包括热重和差示扫描量热法;研究扩散系数常用方法主要是电化学测试方法,如直流法、交流阻抗法等;而采用核磁共振(NMR)技术进行电解质材料物性的研究相对较少.NMR技术[10-12]可以在样品无损条件下,快速地进行相关物理性能测试,得到材料分子微观结构及动力学相关信息,为电解质材料的评价提供了新的测试手段.如:1H NMR和13C NMR可以直观提供有机硅化合物中不同类型氢原子和碳原子分布、互相连接方式、周围化学环境等结构信息[13, 14];二维扩散排序谱(DOSY)可用于研究电解液系统每一个组分的扩散行为,在分子水平研究溶剂分子与离子之间的相互作用,提供评价电解质材料物性的有效数据[15, 16].
有机硅化合物CN(CH2)2SiCH3(OCH2CH2OCH3)2(BNS)作为电解质溶剂,可以增强碳酸盐混合物的电化学稳定性,略微扩大氧化电位[17],在BNS与二元锂盐(LiPF6+LiODFB)组成的电解液中,LiCoO2/石墨全电池表现出优异的循环稳定性和速度能力[18],因此,在制备工业电解液方面很有应用前景.作为电池的安全电解质,BNS由于存在氰基(-CN)和醚键(-O-)基团而显示出高介电常数和高氧化性,但BNS与锂盐或碳酸盐之间的相互作用机理尚未被研究.本文采用NMR技术探究BNS和LiPF6电解液的溶剂化作用、扩散行为和热稳定性等物化特性,为开发具有新型分子结构的有机硅电解质材料提供理论依据,同时也丰富了电解质材料测试表征的手段.
1 实验部分
1.1 实验材料
乙二醇单甲醚、四甲基乙二胺(TMEDA)、氧化亚铜(Cu2O)、二甲基氯硅烷、甲基二氯硅烷、三乙胺(TEA)、六氟磷酸锂(LiPF6)、含0.03% v/v四甲基硅烷(TMS)的CDCl3、丙烯腈和四氢呋喃(THF)购于阿拉丁公司(中国,上海).
1.2 BNS的合成
BNS合成的具体实验过程详见文献[18],合成线路图如下:
1.3 NMR实验
测试仪器为Bruker AVANCE Ⅲ 400型NMR谱仪,配备BBFO-Plus 5 mm探头.
样品溶于CDCl3,以TMS为内标,实验温度为25 ℃.1H、13C、7Li和19F核的共振频率分别为400.15 MHz、100.62 MHz、155.51 MHz和376.48 MHz.1H NMR实验所用脉冲序列为zg30,延迟时间为1.5 s,谱宽为8 012.82 Hz,采集时间为2 s,扫描次数为16.13C NMR实验所用脉冲序列为zgpg30,延迟时间为2 s,谱宽为24 038.46 Hz,采集时间为1.36 s,扫描次数为128.变温NMR实验是N2(气流量为400 L/h)保护下,由25 ℃逐渐升温至85 ℃.DOSY扩散实验的脉冲序列为ledbpgp2s,梯度场宽度p19为600 μs,试探实验脉冲序列为ledbpgp2s1d,p30为试探实验得出的最优参数(p30的设定依据是95%强度梯度下测试的信号强度衰减为2%强度梯度下信号强度的3%~7%,最佳为5%),梯度稳定时间为0.2 ms,扩散时间为20 ms,扩散梯度场强度(gzlvl1)分16步从2%增加到95%. 7Li NMR实验所用脉冲序列为zg30,延迟时间为10 s,谱宽为20 000 Hz,采集时间为1.63 s,扫描次数为16.19F NMR实验所用脉冲序列为zg30,延迟时间为1 s,谱宽为89 285.71 Hz,采集时间为0.73 s,扫描次数为16.
2 结果与讨论
2.1 BNS化合物结构确认
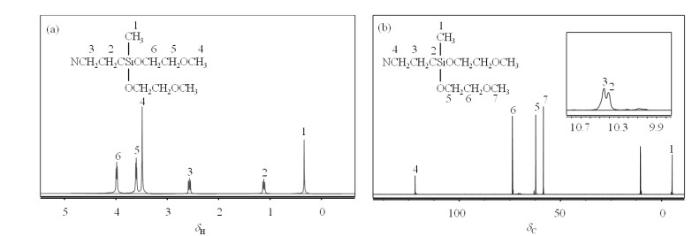
通过反复精馏,BNS经气相色谱(Agilent 7890A)测试,化合物纯度大于99.7%,产率约为86%. 本文通过1H NMR和13C NMR实验确认该化合物的化学结构.BNS的1H NMR如图 1(a)所示,有6组质子信号峰,分别为δH 0.33 (s, 3H, -SiCH3)、1.12 (m, 2H, -SiCH2-)、2.56 (m, 2H, NCCH2-)、3.48 (s, 6H, CH3O-)、3.60 (4H, -CH2O-)和3.98 (4H, -SiOCH2-).图 1(b)展示了BNS的13C NMR谱图,出现了7组碳信号峰:δC - 5.03 (-SiCH3)、10.54 (-SiCH2-)、10.71 (NCCH2-)、58.37 (CH3O-)、62.24 (-SiOCH2-)、73.78 (-CH2O-)和121.27 (-CN).本文合成的BNS的NMR实验值与文献值[19]一致.
图1
图1
BNS的(a) 1H NMR和(b) 13C NMR谱图
Fig.1
(a) 1H NMR and (b) 13C NMR spectra of BNS
2.2 溶剂化作用
溶剂化作用是指溶质-溶剂体系中广义的酸碱相互作用或亲电子体与亲核体的相互作用,溶剂分子通过与离子的相互作用,形成离子与溶剂分子的络合物,溶剂化作用改变了溶剂和离子的结构,而且这种作用的强弱与溶剂分子的介电常数相关,电解液中基础相互作用强弱的变化会显著改变其物理化学性质,因此,锂电池中电解液的溶剂化作用也受到越来越多的关注.本研究通过NMR研究不同浓度电解液的物理化学性质,进一步探究锂盐与溶剂BNS之间的溶剂化作用.
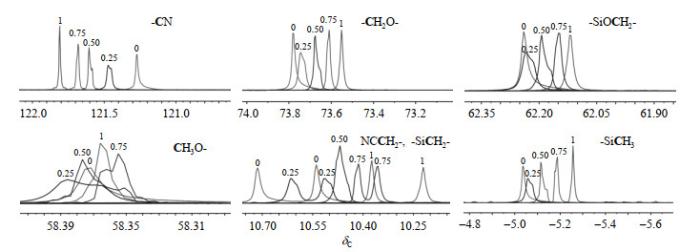
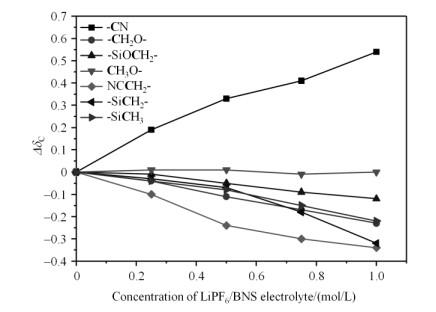
在BNS溶剂中逐渐加入LiPF6,超声溶解0.5 h后形成浓度为0.25 mol/L、0.50 mol/L、0.75 mol/L、1.00 mol/L的LiPF6/BNS电解液,并进行13C NMR实验,研究锂盐浓度对BNS化学位移的影响.BNS各基团13C核的化学位移变化情况如图 2和表 1所示,随着LiPF6浓度的提高,-CN的变化最为明显,特征峰向低场移动,化学位移增大;其他基团-CH2O-、-SiOCH2-、NCCH2-、-SiCH2-、-SiCH3的特征峰向高场移动,化学位移减小,变化幅度相对较小;而CH3O-化学位移相对无明显变化.上述情况说明在BNS众多基团中,-CN优先与LiPF6发生络合配位.由图 2还可以看到随着LiPF6浓度增加,BNS各基团13C NMR信号峰先变宽后变窄,推测在BNS中逐步加入LiPF6,在稀溶液中多个BNS溶剂分子包围在金属Li+周围,Li+不仅与单个BNS分子内的-CN、-O-络合,还同时和围绕在四周的多个BNS分子中的-CN、-O-络合,形成了多个不同键强度的络合键,造成信号峰变宽或裂分;随着Li+浓度不断加大,周围的溶剂分子数目减少,形成结构相对稳定的络合物,上述络合键的数量也迅速下降,表现为信号峰又变窄[20].图 3反映了电解液中BNS各基团13C NMR相对化学位移(△δC,即不同锂盐浓度的电解液与单质溶液中BNS各基团的化学位移的差值)随LiPF6浓度的变化情况.从图 3可以看出,随着LiPF6在电解液中浓度升高,BNS中的-CN、-SiOCH2-、-CH2O-等取代基的化学位移均发生变化,其中-CN的相对化学位移变化最为明显,说明-CN配位能力强于其他基团.可能原因是-CN中碳原子(C)和氮原子(N)通过叁键相连接,叁键使-CN的稳定性增强,其中N原子端形成一孤对电子,该孤对电子容易被金属Li+的d空轨道俘获形成配位.
图2
图2
含有不同浓度LiPF6(0,0.25,0.50,0.75,1.00 mol/L)的电解液中BNS的13C NMR谱图
Fig.2
13C NMR spectra of BNS in electrolytes with different molar concentrations of LiPF6 (0, 0.25, 0.50, 0.75, 1.00 mol/L)
表1 含有不同浓度LiPF6的电解液中BNS各基团的13C NMR化学位移
Table 1
| LiPF6/BNS (mol/L) | δC | ||||||
| -CN | -CH2O- | -SiOCH2- | CH3O- | NCCH2- | -SiCH2- | -SiCH3 | |
| 0 | 121.27 | 73.78 | 62.24 | 58.37 | 10.71 | 10.54 | -5.04 |
| 0.25 | 121.46 | 73.74 | 62.23 | 58.38 | 10.61 | 10.51 | -5.08 |
| 0.50 | 121.60 | 73.67 | 62.19 | 58.38 | 10.47 | 10.47 | -5.12 |
| 0.75 | 121.68 | 73.61 | 62.15 | 58.36 | 10.41 | 10.36 | -5.19 |
| 1.00 | 121.81 | 73.55 | 62.12 | 58.37 | 10.37 | 10.22 | -5.26 |
图3
图3
BNS中各基团的13C NMR相对化学位移(△δC)随LiPF6/BNS电解液浓度变化情况
Fig.3
The 13C NMR relative chemical shifts (△δC) of various groups in BNS varying with the concentration of LiPF6/BNS electrolyte
由图 2和图 3可以看到,相对单质溶液,1 mol/L LiPF6/BNS电解液中BNS的-CN特征峰向低场移动,化学位移值增大0.54 ppm,这说明-CN的高偶极矩使得氰基和Li+之间形成配位键[21],导致-CN中的C原子电子云密度减低,化学位移值增大,且随着Li+浓度升高,离子配位络合程度不断增强,-CN中的C原子化学位移值进一步增大.离子配位络合生成[LiNC]+-,其电场使化学键上电子向邻近的α碳和β碳转移,使得基团NCCH2-和-SiCH2-的化学位移减小,其特征峰分别向高场移动0.34 ppm和0.32 ppm.由表 1、图 2和图 3还可以看到,加入金属锂盐,BNS支链中醚键(-O-)也参与溶剂化作用,-O-和Li+发生配位络合,络合引发的电场效应使得-CH2O-、-SiOCH2-对应的化学位移略有降低;CH3O-的化学位移变化不大,推测BNS两条长支链的空间位阻效应降低了CH3O-基团中的-O-与Li+的配位络合程度.
综上表明LiPF6/BNS电解液发生了溶剂化效应,BNS上的-CN和-O-均与金属Li+发生配位络合,且具有强偶极矩的-CN优先与Li+形成络合键,BNS分子中存在的-CN和-O-增强了LiPF6与溶剂BNS之间的相互作用,从而提高了BNS的介电常数,促进了锂盐的离解.
2.3 扩散行为
扩散是物质的迁移现象,其中液体扩散系数是研究分子传质过程的重要参数,它可定性和定量反映如分子大小、状态以及分子间作用力等性质.扩散系数的大小主要取决于扩散物质和扩散介质的种类、温度和压力.DOSY是目前测量溶液样品的自扩散系数(D)的一个重要方法,DOSY实验中扩散系数由Stokes-Einstein方程计算得出,公式如下[22]:
I为加梯度场后的信号强度,
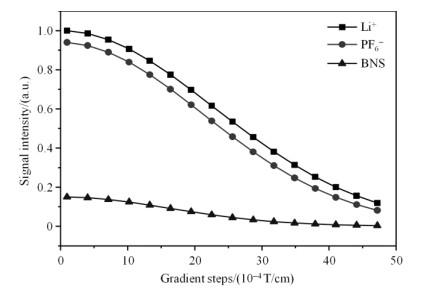
1 mol/L LiPF6/BNS电解液的DOSY实验拟合如图 4所示,根据脉冲梯度场g的变化可采集到对应衰减程度不同的谱峰信号强度,积分区域16个点,由(1)式可知,I与D呈负对数关系:I越大,D反而越小.根据Stokes-Einstein公式,将实验中不同梯度场强度下测得的谱峰信号强度I代入(1)式,通过指数拟合分别得出电解液中BNS、Li+、PF6-的扩散系数,如表 2所示.由图 4和表 2可知BNS电解质材料的扩散系数是7.30×10-12 m2/s,当加入LiPF6形成1 mol/L LiPF6/BNS电解液后,BNS扩散系数降低为4.79×10-12 m2/s,Li+扩散系数为2.50×10-12 m2/s,PF6-扩散系数为2.88×10-12 m2/s,电解液中各个组分扩散系数大小排序为:
图4
图4
1 mol/L LiPF6/BNS电解液中各组分的DOSY拟合
Fig.4
DOSY experiments of each component in 1 mol/L LiPF6/BNS electrolyte
表2 BNS和不同浓度LiPF6/BNS电解液各组分的扩散系数
Table 2
| LiPF6/BNS (mol/L) | D/(×10-12 m2/s) | ||
| BNS | Li+ | PF6- | |
| 0 | 7.30 | / | / |
| 0.5 | 5.35 | 2.25 | 2.47 |
| 1.0 | 4.79 | 2.50 | 2.88 |
由表 2中BNS和不同浓度LiPF6/BNS电解液DOSY实验结果,可知0.50 mol/L LiPF6/BNS电解液中Li+扩散系数为2.25×10-12 m2/s,当LiPF6/BNS电解液浓度升高到1 mol/L时,Li+扩散系数升高为2.50×10-12 m2/s,说明在LiPF6/BNS的稀溶液中存在大量自由溶剂分子BNS,溶剂分子BNS的扩散速度大于Li+的扩散速度,溶剂分子中-CN、-O-与Li+之间相互作用,形成多个溶剂分子和Li+配位的溶剂化结构,随着Li+浓度升高,溶剂分子BNS与Li+形成的溶剂化结构逐渐转变为更为稳定的结构,Li+的扩散速度也相应变快.
以上表明BNS化合物由于存在-CN和-O-与Li+形成的溶剂化结构促进了锂盐的离解和扩散,加快了Li+的扩散速度,提高了电解液的电导率,这也与LiPF6/BNS电解液溶剂化作用分析结果一致.
2.4 电解液热稳定性
锂离子电池的热稳定性受正极、负极及电解液三种因素的影响,电解液的热稳定性好,不仅能延长电池循环寿命,提高电池快速充放电能力,而且能提高电池的安全性.LiPF6是锂离子电池中最常用的盐,因为它在有机电解液中具有很高的溶解性和良好的离子导电性.然而,LiPF6的热稳定性较差,易发生分解,反应如(2)式所示,在较高温度下会产生越来越多的LiF和PF5[23].
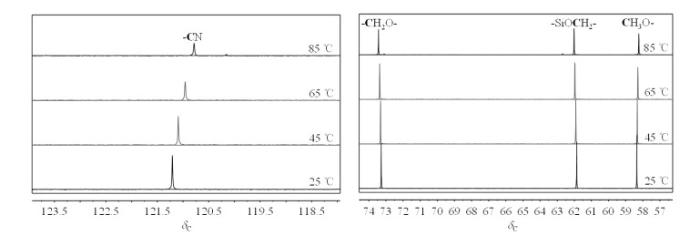
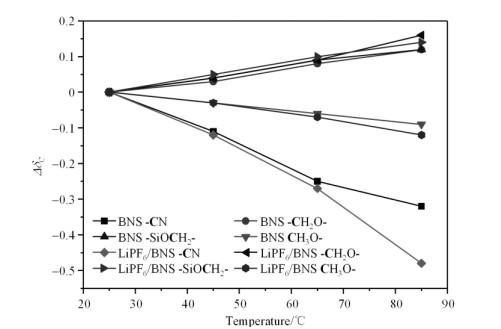
实验采用变温13C NMR研究1 mol/L LiPF6/BNS电解液的热稳定性.当温度由25 ℃逐渐升高85 ℃时,电解液中BNS的13C特征峰化学位移变化情况如图 5所示.可以看到随LiPF6/BNS电解液温度升高,-CN的化学位移减小;-CH2O-、-SiOCH2-的化学位移略有增大,CH3O-的化学位移略有减小.图 6反映了BNS单质溶剂和1 mol/L LiPF6/BNS电解液中相关基团13C相对化学位移随温度变化情况:低温下,电解液中的BNS各基团的△δC与BNS单质溶剂中对应基团的△δC变化基本一致,-CN和CH3O-的化学位移减小,-CH2O-和-SiOCH2-的化学位移略有增大.当温度由65 ℃进一步升高,电解液中相关基团13C NMR化学位移变化明显大于BNS单质溶剂,并且随温度升高这种变化更加明显,其中△δ-CN变化最为显著.由上述情况推测LiPF6和BNS之间形成了络合键,且在各基团中,Li+优先与-CN发生络合,Li+与-O-形成的络合键数量相对较少.结合图 5和图 6,可以看到LiPF6与BNS之间形成的络合键增强了电解液的稳定性,且二者间的络合主要为Li+与-CN之间的络合;温度在65 ℃下电解液的络合结构相对稳定,当温度升高到65 ℃以上,LiPF6和BNS之间络合键部分发生断裂,-CN的化学位移明显减小.此外,由图 5还可以看到较高温度下BNS对应的特征峰强度略微变弱,说明高温下BNS化合物有一定程度的分解.
图5
图5
不同温度下,1 mol/L LiPF6/BNS电解液中BNS的13C NMR谱图(δC 50~125)
Fig.5
13C NMR spectra (δC 50~125) of BNS in 1 mol/L LiPF6/BNS electrolyte at different temperatures
图6
图6
BNS和1 mol/L LiPF6/BNS电解液中BNS相关基团的13C NMR相对化学位移(△δC)随温度的变化
Fig.6
13C NMR relative chemical shifts (△δC) of related groups in BNS with and without 1 mol/L LiPF6 electrolyte changing with temperatures
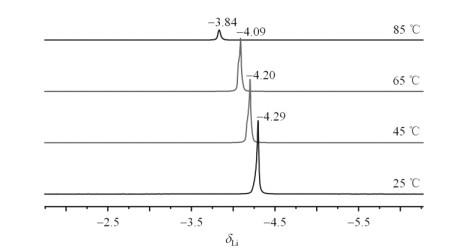
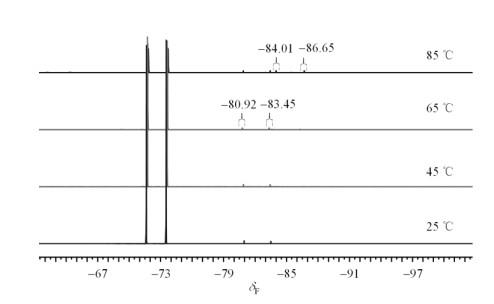
LiPF6/BNS电解液的热稳定性在一定程度上受电解液中Li+的配位结构及BNS分子浓度的影响,而决定Li+的配位结构及BNS分子浓度的因素有锂盐浓度、溶剂和阴离子结构.为了进一步研究LiPF6/BNS组成电解液的热稳定性,我们进行了变温7Li NMR实验.电解液中7Li NMR如图 7所示,温度由25 ℃逐渐升高65 ℃时,Li+对应的特征峰峰面积变化不大,由于温度升高,金属Li+运动加快,Li+与BNS之间的络合键部分断裂,化学位移向低场移动,由δLi - 4.29增大为δLi - 4.09,温度进一步升高到85 ℃,Li+特征峰面积明显变小,说明较高温度下电解液中的LiPF6本身可能发生了分解[23]. 为了证实上述推论,补充了变温19F NMR实验.1 mol/L LiPF6/BNS电解液的19F NMR谱如图 8所示,25 ℃至65 ℃变温条件下,化学位移在δF - 73附近出现二重强峰为PF6-,同时在δF -80.92、-83.45附近出现的两组弱吸收峰为杂质O=PF2(OH)的特征峰,当温度进一步升高到85 ℃时,化学位移在δF -73附近二重强峰峰强度明显变弱,在δF -84.01、-86.65也出现O=PF3双重共振峰[24],上述情况表明在较高温度下,LiPF6发生了分解,产生多种化学结构,导致P元素具有多种化学环境,分解的产物主要是O=PF2(OH)和O=PF3.
图7
图7
不同温度下,1 mol/L LiPF6/BNS电解液的7Li NMR谱图
Fig.7
7Li NMR spectra of 1 mol/L LiPF6/BNS electrolyte at different temperatures
图8
图8
不同温度下,1 mol/L LiPF6/BNS电解液的19F NMR谱图
Fig.8
19F NMR spectra of 1mol/L LiPF6/BNS electrolyte at different temperatures
上述变温NMR实验结果表明,电解液中LiPF6与BNS形成了以Li+与-CN之间的络合为主的络合物,这种络合一定程度上提高了电解液的稳定性;电解液在65 ℃以下并没有显示出明显的分解;随着电解液温度进一步升高,Li+与BNS之间的络合键部分断裂,电解液中LiPF6发生明显分解.综上证明,在高温下LiPF6的分解是电解液失效的主要因素.
3 结论
本文采用多种NMR技术研究了有机硅电解质材料BNS相关物化特性,展示了NMR技术的优势,丰富了电解质材料测试表征的手段.研究表明BNS与LiPF6之间具有溶剂化效应,BNS中存在诱导偶极氰基(-CN)和醚键(-O-)可与锂盐LiPF6形成络合物,且氰基(-CN)配位能力优于醚键(-O-).这种相互作用促进了LiPF6的离解和扩散,提高了电解液的电导率,同时也使电解液(LiPF6/BNS)在65 ℃以下表现出较好的热稳定性,证明高温下LiPF6的分解是电解液失效的主要因素.实验结果为开发设计具有新型分子结构的电解质化合物及促进其性能的提升提供了理论依据.
无
参考文献
Research progress of materials for power lithium-ion battery
[J].
锂离子动力电池材料研究进展
[J].
Enabling LiTFSI-based electrolytes for safer lithium-ion batteries by using linear fluorinated carbonates as (Co) solvent
[J].
Flexible thermoelectric materials based on conducting polymers doped with silicone polymer electrolyte
[J].DOI:10.1080/15421406.2019.1645467
Binder-free silicon anodes wrapped in multiple graphene shells for high-performance lithium-ion batteries
[J].DOI:10.1016/j.jpowsour.2020.229350 [本文引用: 1]
Synthesis of cyano containing organosilicon based electrolytes
[J].
含氰基有机硅电解质的合成
[J].
Improvement of lithium-ion battery performance at low temperatureby adopting polydimethylsiloxane- based electrolyte additives
[J].DOI:10.1016/j.electacta.2014.05.054 [本文引用: 1]
Effect of nitrile group functionalized organosilicon as electrolyte additive on low-temperature performance of LiFePO4battery
[J].
腈基功能化有机硅电解液添加剂对LiFePO4电池低温性能的影响
[J].
The progress in exploration of organosiloxane used in the electrolyte to improve the lithium batteries' safety performance
[J].DOI:10.3969/j.issn.1001-9731.2014.22.001 [本文引用: 1]
有机硅在锂离子电池电解质中的应用
[J].DOI:10.3969/j.issn.1001-9731.2014.22.001 [本文引用: 1]
Electrochemical performance of activated graphene powder supercapacitors using a room temperature ionic liquid electrolyte
[J].
基于室温离子液体的活化石墨烯粉末超级电容储能性能
[J].
Progresses in solid-state NMR studies on carbon anode materials for lithium/sodium-ion batteries
[J].
固体核磁共振技术在锂/钠离子电池碳负极中的应用及研究进展
[J].
Molecular structure, spectroscopic (FT-IR, FT-Raman, NMR, UV-VIS), chemical reactivity and biological examinations of ketorolac
[J].DOI:10.1016/j.molstruc.2020.128040 [本文引用: 1]
Structure and configuration analyses of a nucleating agent for isotactic polypropylene crystallization
[J].
规聚丙烯成核剂的结构和构型分析
[J].
Homogeneous and fast ion conduction of PEO-based solid-state electrolyte at low temperature
[J].
Determination of apparent protein molecular weight in solution by diffusion ordered NMR spectroscopy
[J].
扩散序谱(DOSY)实验测定缓冲体系中蛋白质表观分子量
[J].
Application progress of nuclear magnetic resonance diffusion ordered spectroscopy
[J].DOI:10.3969/j.issn.1004-4957.2020.08.017 [本文引用: 1]
核磁共振扩散序谱的研究及应用进展
[J].DOI:10.3969/j.issn.1004-4957.2020.08.017 [本文引用: 1]
Improve safety of high energy density LiNi1/3Co1/3Mn1/3O2/graphite battery using organosilicon electrolyte
[J].DOI:10.1016/j.electacta.2018.11.036 [本文引用: 1]
Organosilicon compounds containing nitrile and oligo(ethylene oxide) substituents as safe electrolytes for high-voltage lithium-ion batteries
[J].DOI:10.1016/j.jpowsour.2013.12.087 [本文引用: 2]
Spectroscopic study of ion-solvent and ion-ion interactions in lithium battery electrolyte solution Ⅶ. LiBF4/g-butyrolactone
[J].DOI:10.3969/j.issn.1000-2367.2002.04.036 [本文引用: 1]
锂电池电解质溶液中离子-溶剂和离子-离子相互作用的谱学研究Ⅶ. LiBF4/g-丁内酯
[J].DOI:10.3969/j.issn.1000-2367.2002.04.036 [本文引用: 1]
Nitrile-modified 2, 5-di-tert-butyl-hydroquinones as redox shuttle overcharge additives for lithium-ion batteries
[J].
过充保护添加剂氰基功能化2, 5-二叔丁基对苯二酚的合成及其在锂离子电池中的应用
[J].
Effects of digital resolution on diffusional dimension in DOSY experiments
[J].
扩散序谱(DOSY)实验中扩散系数维数字分辨率的影响
[J].
Lithium-ion conducting electrolyte salts for lithium batteries
[J].DOI:10.1002/chem.201101486 [本文引用: 2]
Study of lithium hexafluorophosphate by NMR spectroscopy
[J].DOI:10.3969/j.issn.1001-9677.2014.14.037 [本文引用: 1]
六氟磷酸锂的核磁共振波谱研究
[J].DOI:10.3969/j.issn.1001-9677.2014.14.037 [本文引用: 1]